お知らせ
■NEWS 「タケキャブ」の副作用に「汎血球減少、無顆粒球症、白血球減少、血小板減少」を追加
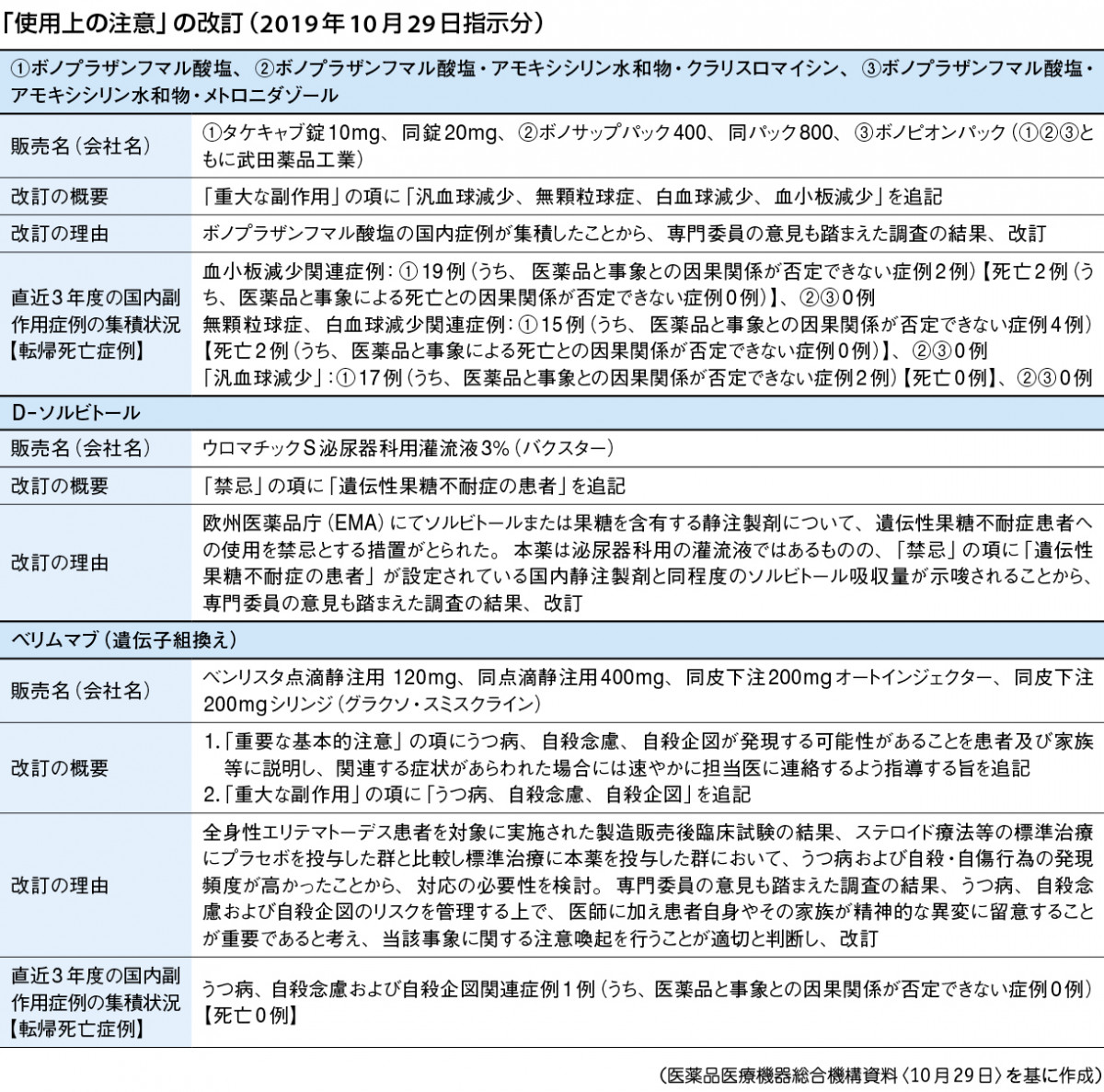
厚生労働省は10月29日付で、日本製薬団体連合会に対し、酸分泌抑制薬のタケキャブ、ボノサップ、ボノピオン(一般名:ボノプラザンフマル酸塩含有製剤)などの添付文書改訂を指示する通知を発出した(下掲)。
ボノプラザンフマル酸塩含有製剤では、「重大な副作用」の項に「汎血球減少、無顆粒球症、白血球減少、血小板減少」を追記する。改訂は、国内症例の集積を受けたもの。タケキャブの直近3年度の国内副作用症例の集積状況は、「血小板減少関連症例」が19例(うち医薬品との因果関係が否定できない症例2例)、「無顆粒球症、白血球減少関連症例」が15例(うち医薬品との因果関係が否定できない症例4例)、「汎血球減少」が17例(うち医薬品との因果関係が否定できない症例2例)。
泌尿器科用灌流液の「D-ソルビトール」(ウロマチックS泌尿器科用灌流液3%)では、「禁忌」の項に「遺伝性果糖不耐症の患者」を追記する。