お知らせ
イグザレルトの適応追加は継続審議 - 新薬情報
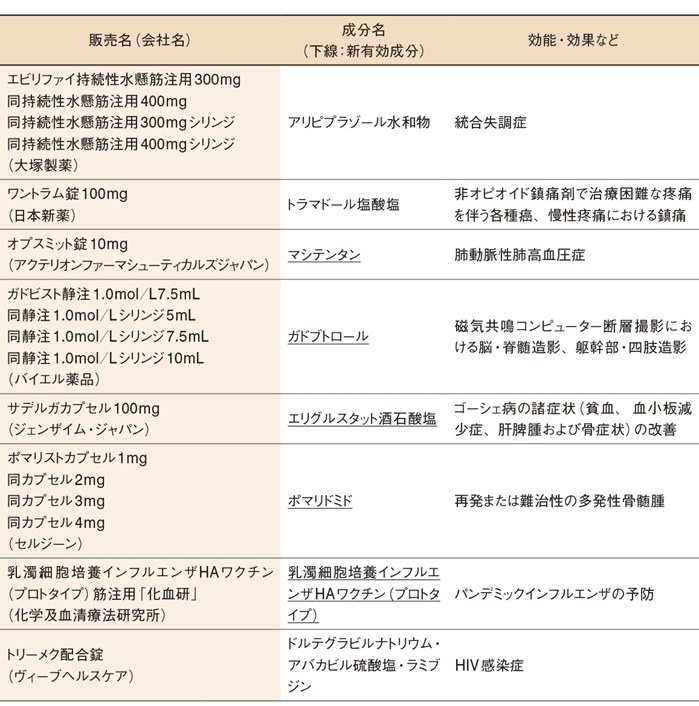
厚生労働省の薬事・食品衛生審議会医薬品第一部会と第二部会が2月20日と26日にそれぞれ開かれ、下掲の医薬品8成分17品目について、承認して差し支えないとの結論をまとめた。
第一部会では1製品の承認了承が見送られ、継続審議となった。見送りになったのは、バイエル薬品の経口抗凝固薬「イグザレルト錠」への「深部静脈血栓症」「肺血栓塞栓症」の適応追加。同省医薬食品局の担当者は、継続審議となった理由について「承認の可否を判断するに当たり、懸念されることがあったため」と説明しており、詳細は明かしていない。
新型インフルのプロトタイプワクチンが了承
「乳濁細胞培養インフルエンザHAワクチン(プロトタイプ)筋注用『化血研』」は、新型インフルエンザの発生に備え、あらかじめ株を特定せずに製造方法や品質管理の内容を承認するもの。新型インフルエンザ発生時にパンデミックワクチン製造までの期間を短縮し、迅速に供給できるようにする。同様のプロトタイプワクチンは既に2品目が承認されている。