お知らせ
■NEWS 【薬価収載】ロナセン、ネスプなどに後発品―5成分48品目が初収載
厚生労働省は6月14日付で、86成分264品目の後発医薬品を薬価基準に収載した。
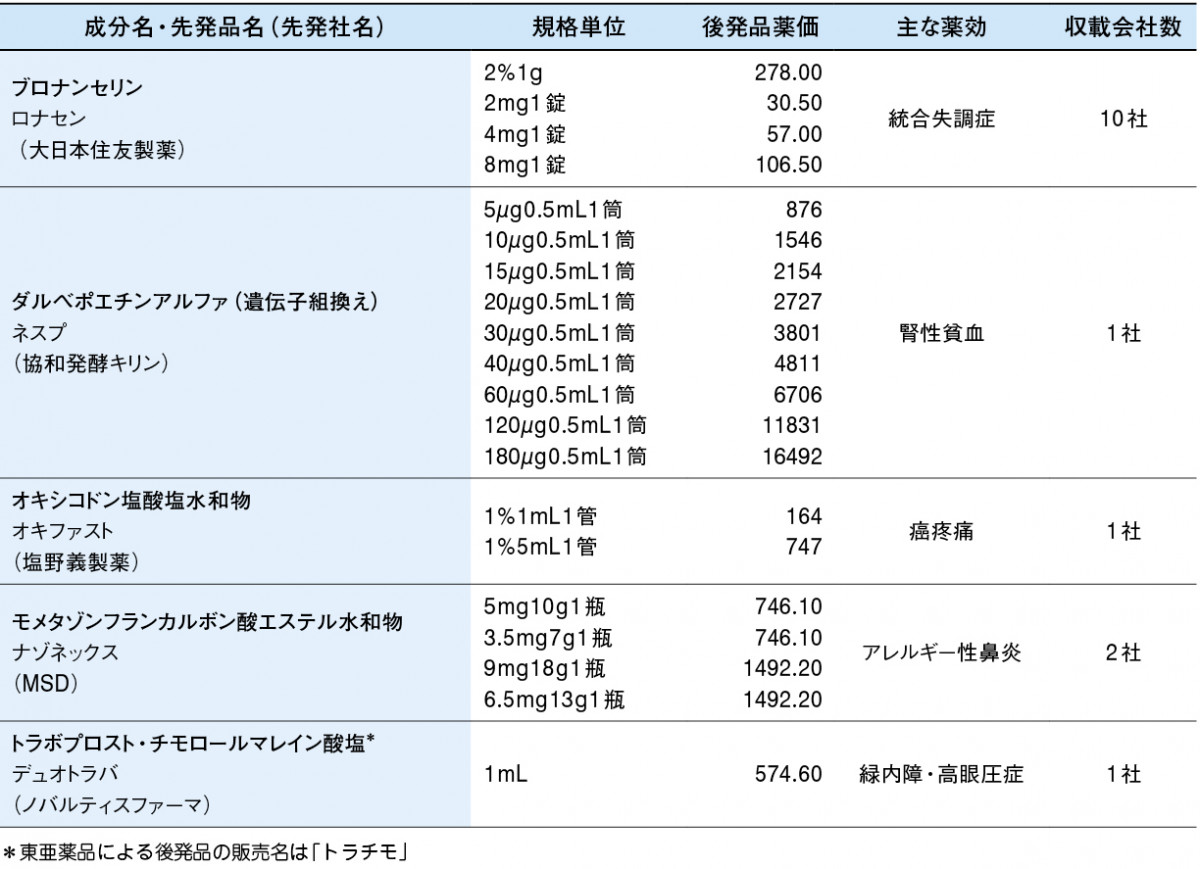
今回、後発品が初めて収載されたのは、統合失調症治療薬「ロナセン」(ブロナンセリン)、腎性貧血治療薬「ネスプ」(ダルベポエチンアルファ)、癌疼痛治療薬「オキファスト」(オキシコドン塩酸塩水和物)、アレルギー性鼻炎治療薬「ナゾネックス」(モメタゾンフランカルボン酸エステル水和物)、緑内障治療薬「デュオトラバ」(トラボプロスト・チモロールマレイン酸塩)の5成分48品目(表)。
■ロナセンなど3成分にAG
有効成分・原薬・添加物・製法などが先発品と同一であるオーソライズド・ジェネリック(AG)が収載されたのは、①ロナセン、②ネスプ、③ナゾネックス―の3成分。それぞれのAGの製造販売元は、①がDSファーマプロモ、②が協和キリンフロンティア、③がキョーリンリメディオ。
後発品薬価は、原則として先発品薬価の0.5掛けとなる。先発品が新薬創出等加算の対象品目である場合は加算分を控除した上で算定される。このルールにより、ロナセンとナゾネックスの後発品薬価は先発品の40%程度になった。
■ネスプAGの薬価は先発品の6~7割に
ネスプのAGは、先発会社の協和発酵キリンの完全子会社である協和キリンフロンティアが製造する、いわゆるバイオセイム。バイオセイムの薬価については、今年3月の中央社会保険医療協議会薬価専門部会で、先発品と同等の有効性・安全性が治験等で確認されたバイオシミラーと同様に0.7掛けで算定することとされた。ネスプのAGの薬価は先発品の約63~69%となっている。
ただし、この対応はあくまで「暫定的な措置」として了承されたもの。薬価専門部会では、委員から、完全子会社を通じて先発品と同じ製品を製造販売するというバイオセイムのあり方や企業戦略に「違和感」を表明する声が続出した。2020年度診療報酬改定に向け、引き続き対応が検討される見通しだ。