お知らせ
【Breakthrough 医薬品研究開発の舞台裏(1)浜谷 越郎(アステラス・アムジェン・バイオファーマ/骨領域シニアメディカルアドバイザー)】〈骨形成促進〉と〈骨吸収抑制〉両方の作用を持つイベニティは、骨粗鬆症治療の「最終兵器」
製薬企業に対する医療現場の期待・要望でいつも上位に来るのが「新薬開発への期待」。3月に実施した本誌アンケートでは、新薬開発を期待する領域として「精神・神経」「がん」「腎・内分泌代謝」「感染症」に次いで「整形外科」を挙げる声も多く寄せられた。
各メーカーの開発担当者へのインタビューを通じて「医薬品研究開発の舞台裏」に迫る本シリーズの第1回は、整形外科領域の代表的疾患である骨粗鬆症の新薬「イベニティ」(一般名:ロモソズマブ)を取り上げ、開発に携わったアステラス・アムジェン・バイオファーマ(AABP)の浜谷越郎氏にイベニティの特性、開発の経緯などを聞いた。

はまや えつろう:昭和薬科大卒。薬剤師。東邦薬品、クレハ、日本イーライリリー勤務を経て、2014年4月より現職。
─イベニティ(2019年3月発売)は従来の骨粗鬆症治療薬と主にどこが違うのでしょうか。
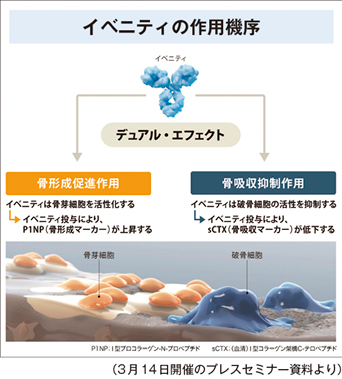
浜谷 これまでの骨粗鬆症治療薬は、破骨細胞の活性を制御する、骨芽細胞の機能を促進するといった細胞レベルの話が多かったのですが、イベニティの場合は、骨形成促進に関わるWnt(ウイント)シグナルを阻害するスクレロスチンという糖蛋白をターゲットにして創薬を進めました。そこが全く新しいところです。
従来の治療薬は、骨吸収抑制か骨形成促進いずれかの作用を主として持っていますが、イベニティは骨形成促進作用と骨吸収抑制作用のデュアル・エフェクトを持っています。臨床試験では1年という短期間で骨粗鬆症治療の最終目標である骨折発生率の有意な低下が認められました。骨粗鬆症治療薬としては私はこれが“最終兵器”になると考えています。
審査の過程で日本が米国を追い抜く
─どういう経緯で開発が始まったのですか。
浜谷 Wntシグナル経路の骨代謝への関わりが明らかになってきたのは2000年代に入ってから。WntシグナルへのスクレロスチンとSOST遺伝子の関与も分かってきて、そこに着目した創薬をアムジェンとユーシービーとで始めました。
─浜谷さんはいつ頃から関わり始めたのですか。
浜谷 私は、AABPに入社した2014年4月からです。それ以前に日本イーライリリーで骨粗鬆症治療薬の研究開発に取り組んでいた頃、「エビスタ」(一般名:ラロキシフェン)の開発で1997年から2000年代初頭にかけてグローバルと議論してきた経験がイベニティの臨床開発で役立ちました。特にビタミンDやカルシウムに対する欧米と日本の意識の違いや、骨密度の変化率で民族間の類似性を評価するときの落とし穴を知っていたことは大きかったです。
─イベニティは世界に先駆けて日本で発売されましたが、もともとそういう計画だったのですか。
浜谷 米国のFDAへの申請のほうが先でしたが、審査の過程で日本が追い抜く形になりました。日本での承認に続き米国でも4月9日に承認されました。
─イベニティの効能・効果に関連する使用上の注意に「海外で実施された試験で、心血管系事象の発現割合がアレンドロン酸ナトリウム群に比較して高い傾向が認められている」と記載されていますが、臨床医はこの点をどう考えればいいですか。
浜谷 重篤な心血管系有害事象の発現率に関して、プラセボ対照で実施した「FRAME試験」(7180例、うち日本人492例)ではイベニティ群とプラセボ群で不均衡は認められなかったのですが、標準治療薬アレンドロネート(アレンドロン酸ナトリウム)を対照として欧州で実施した「ARCH試験」(4093例、日本人の登録なし)ではイベニティ群2.5%、アレンドロネート群1.9%と不均衡が認められました。
アレンドロネートを含むビスホスホネート製剤では以前より心血管系事象を低下させるという報告が散見され、他の骨粗鬆症治療薬の臨床試験データや疫学データと比較すると、イベニティ群の発現率は同等かむしろ低い。臨床医の先生方にはその辺りの事実を正確にお伝えしていきたいと考えています。
閉経後女性のアウェアネスをどう変えるか
─これまで長年にわたり骨粗鬆症治療薬の開発に携わる中で転機のようなものはありましたか。
浜谷 開発担当者としての意識が変わったのは、イーライリリー時代にエビスタの臨床使用が可能になってからです。それまでは「臨床開発部門の打ち出す戦略が最上位で、営業担当者はそれに従って先生方に適正使用をおすすめすればいい」といった考え方を持っていました。しかしエビスタが世に出て、全国の営業担当者会議などでお話しする機会が増え、MR(医薬情報担当者)と一対一で言葉を交わすうちに、MRの皆さんが毎日命がけで臨床医の先生方と接して活動しているということが身に染みて分かり、この人たちのために自分のメディカルサイエンスを活用していかなければいけないと考えるようになりました。
メディカル担当として医療現場に呼ばれ、自分の持つ知識で問題を解決し、自社製品の採用に至ったときに、現場のMRから本気の「ありがとうございました」をいただいた瞬間以上の喜びはなかったです。
─骨粗鬆症治療薬で次に開発するものがないとすると、今後は啓発に力を入れていくことになりますか。
浜谷 啓発活動にはこれまでも研究開発と並行して取り組んできました。
現在、骨粗鬆症患者はおよそ1280万人と推定されていますが、実際に治療されている方はその中の2割ともいわれています。製薬メーカーはその2割の患者を取り合うのではなく、残りの8割の患者を骨折のリスクからどう救うかを考え、閉経後女性の意識・ア ウェアネスを変えていかないといけません。
これまでもテレビCMを含めメーカーによる啓発活動が行われてきましたが、一般の女性の間には骨粗鬆症というと「老化・衰弱」のイメージがあり、実際に骨折の危険性が高い状態にあっても「自分ではない」という意識があります。そこにどうアプローチをしていくか。製薬会社の中からは出ないようなアイデアがないと踏み込んでいけないんじゃないかと考えています。
─最後に現場の臨床医へのメッセージを。
浜谷 開発のスピードが問われ、治験もCRO(開発業務受託機関)が調査・選定した施設で集中的に行われるようになると、オピニオンリーダーの先生が発売まで使用経験がないというケースが起きます。イベニティでは幸い、オピニオンリーダーの先生も治験に参加しアドバイザーになっていただけましたが、治験実施施設とオピニオンリーダーの乖離は大きな問題です。
オピニオンリーダーの臨床医の先生方にもぜひ積極的に参加いただき、その中で治験が円滑に実施できるような方向に変わっていってほしいと思っています。


































