お知らせ
■NEWS 変形性関節症治療薬「ジョイクル」で安全性速報─重篤なショックなど10例報告

小野薬品工業と生化学工業は6月1日、厚労省からの指示を受け、変形性関節症治療薬「ジョイクル関節注30mg」(一般名:ジクロフェナクエタルヒアルロン酸ナトリウム)によるショック、アナフィラキシーについて安全性速報(ブルーレター)を発出し、医療関係者などへの注意喚起を行った。
ジョイクルについては、今年3月の承認取得以降5月28日までに重篤なショック、アナフィラキシーの症例が10例報告(推定使用患者数約5500人)。このうち1例は因果関係不明ながら死亡に至っている。

安全性速報は、これらの報告を踏まえ、添付文書への「警告」欄新設などの情報提供をした上で、①緊急時に十分な対応ができる準備をした上で投与する、②投与後少なくとも30分間は医師の管理下で患者の状態を観察する、③患者・家族に対しショック、アナフィラキシー発現の可能性があることやその徴候・症状について十分に説明し、異常が認められた場合は速やかに受診するよう指導する─の3点について注意喚起している。
■ヒアルロン酸にジクロフェナクを化学結合
ジョイクルは、ヒアルロン酸にジクロフェナク(抗炎症薬)を化学結合した薬剤。「変形性関節症(膝関節、股関節)」の治療薬として承認され、5月19日から小野薬品が販売している。
ジョイクルについては、臨床試験成績を踏まえ、承認当初から添付文書で重大な副作用としてショック、アナフィラキシーに関する注意喚起がなされ、成分等に対し過敏症の既往歴のある患者は禁忌とされていた。
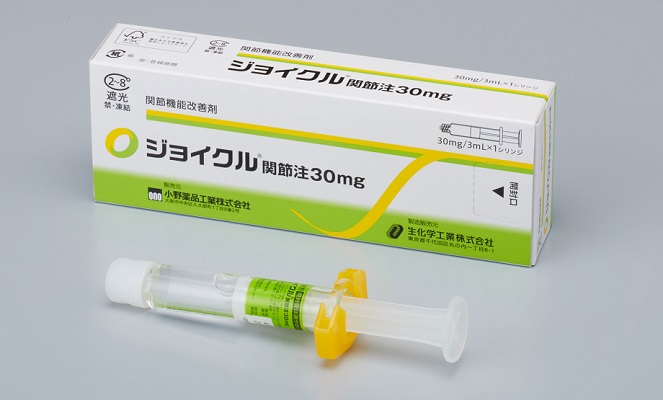
関節機能改善剤「ジョイクル関節注30mg」