お知らせ
2章 疾患別のステロイドの使い方 A 膠原病:11.ベーチェット病
- 登録日:
- 2022-12-20
- 最終更新日:
- 2023-04-11
ステロイド治療の心構え
眼病変,血管病変,消化管病変,神経病変ではステロイド抵抗性を示したり,減量過程で再燃したりすることが少なくありません。
コルヒチン,免疫抑制薬,TNF阻害薬などを併用して,ステロイドの減量・中止をめざします。
1 疾患の概要
▪ベーチェット(Behçet)病は,口腔粘膜の再発性アフタ性潰瘍(以下,再発性口腔アフタ),陰部潰瘍,皮膚病変,眼病変を特徴とする原因不明の炎症性疾患です。
▪Th1細胞,Th17細胞,γδT細胞によりマクロファージが活性化し,好中球が遊走して炎症が惹起されていると考えられています1)。
▪Chapel Hill Consensus Conferenceという国際的な血管炎の会議では,ベーチェット病は様々なサイズ・種類の血管を侵しうる“variable vessel vasculitis”に分類されています2)。
▪トルコを筆頭に中東諸国で罹患率が高く,罹患率が高い地域が日本を含む東アジアに広がっていることから,「シルクロード病」とも呼ばれます。
▪日本人ではHLA-B51に加えて,HLA-A26との関連が示されています3)。
2 どういうときにステロイドを使うか?
▪全例にステロイドを使う必要はありません。
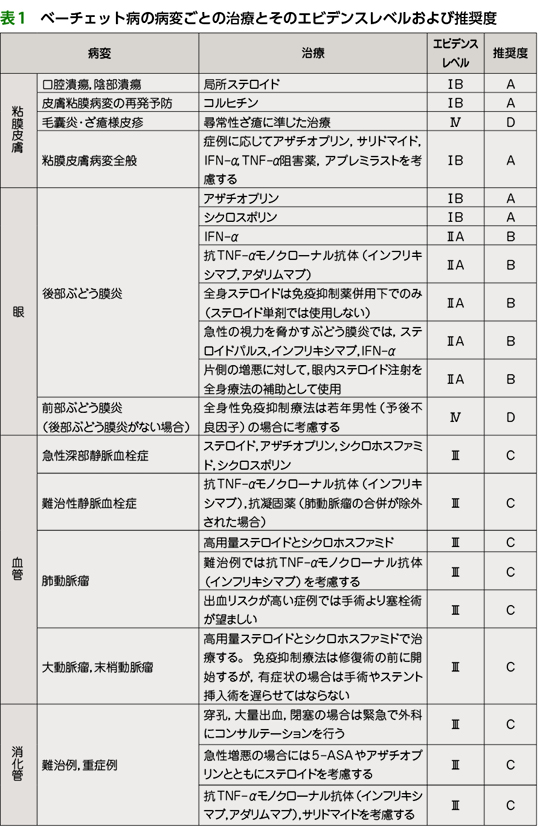
▪出現頻度の高い粘膜皮膚病変は局所ステロイド,コルヒチンを第一選択にします(表1)4)。
▪眼病変(後部ぶどう膜炎),血管病変,消化管病変,神経病変を有する場合は不可逆的な臓器障害に陥るリスクが高いため,全身ステロイドを投与します(表1)4)。
▪臓器障害がなくても,発熱などの全身症状を認める場合は,短期間全身ステロイド投与を行うことがあります。
▪関節炎に対してもコルヒチンを第一選択とします(表1)4)。単関節炎の場合はステロイド関節内注射も選択肢に入れます。発熱を伴っていれば,全身ステロイド投与をすることで関節炎も改善します。
3 ステロイドの根拠は?
▪ステロイドの根拠は専門家の経験,症例報告,わずかな無作為化比較対照試験に基づいています。
▪後部ぶどう膜炎を対象とした無作為化二重盲検試験では,ステロイドパルス療法を施行した群で視力が有意に改善し,再燃が少なかったことが示されています5)。
4 ステロイドの初期用量は?
▪発熱などの全身症状があり主要臓器病変がない場合は,PSL 0.4~0.5mg/kg/日程度で治療を開始します。
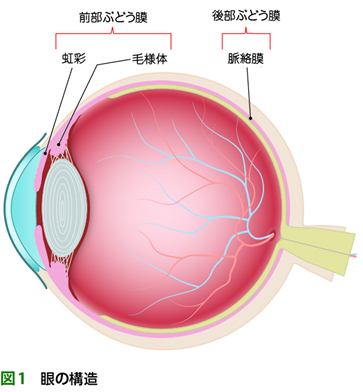
▪軽度の前部ぶどう膜炎(図1)に対しては,眼科医の判断のもとにステロイド点眼薬(例:0.1%ベタメタゾン点眼液1日1~16回)で治療を開始します。重度の前部ぶどう膜炎に対してはステロイド点眼薬に加えてステロイド(例:デキサメタゾン2mg/0.5mL)を結膜下注射します6)。前部ぶどう膜炎に対しては,基本的に全身ステロイド投与を行いませんが,若年男性の場合は予後不良因子とされ,全身ステロイド投与を含む免疫抑制療法を考慮することがあります4)。
▪後部ぶどう膜炎,汎ぶどう膜炎(前部+後部ぶどう膜炎)(図1)の場合は,PSL 1mg/kg/日による全身ステロイド投与を行います。視力低下のおそれがある場合は,ステロイドパルス療法を行います4)。片側の場合は,ステロイドの硝子体内注射や後部テノン囊下(強膜の外側)注射を行うことがあります。
▪急性深部静脈血栓症に対しては,PSL 0.5~1mg/kg/日程度で治療を開始します7)。
▪肺動脈を含む動脈病変の場合は,PSL 1mg/kg/日で治療を開始します。肺動脈瘤や重篤病変ではステロイドパルス療法を行います7)。
▪消化管病変の場合は,PSL 0.5~1mg/kg/日で治療を開始します8)。
▪急性の脳実質病変,髄膜炎に対しては,PSL 0.5~1mg/kg/日程度で治療を開始します。重症,治療抵抗性の場合はステロイドパルス療法を行います9)。
MEMO
頻度の高い表在性血栓性静脈炎は「粘膜皮膚病変」に含まれ,深部静脈血栓症を「血管病変」として考えます。
ベーチェット病の急性深部静脈血栓症は静脈炎によって生じるため,抗凝固療法単剤よりステロイドなどの免疫抑制薬を併用したほうが血栓症の再発が少ないことが示されています4)。

実臨床では,急性深部静脈血栓症に対してはステロイドなどの免疫抑制療法に抗凝固療法を併用することが多いのですが,抗凝固療法を併用せずに免疫抑制療法のみでも治療効果は変わらないとする報告もあります4)。
ピットフォール
➡ベーチェット病に消化管病変が出現した場合は,安易に腸管ベーチェット病と判断せず,内視鏡でNSAIDs潰瘍,炎症性腸疾患,結核などの感染症を除外する必要があります。
5 治療への反応性は?
▪臓器障害がない場合,発熱などの全身症状はステロイド投与後に速やかに改善します。髄膜炎もステロイド投与後に速やかに改善することが多いです。
▪それ以外の臓器病変(眼,血管,消化管,神経)はステロイドに治療抵抗性を示すことが少なくありません。
6 寛解導入療法はステロイド単剤でよいか?
▪ベーチェット病に対しては,ステロイド単剤で治療することはほとんどありません。
▪口腔潰瘍は必発であるため,ほぼ全例でコルヒチンを投与します。コルヒチンは口腔潰瘍以外の粘膜皮膚病変や関節炎にも有効です。
▪口内炎に対してはアプレミラストも有効です10)。
▪前部ぶどう膜炎に対しては,炎症により虹彩が水晶体に癒着する虹彩後癒着,続発性緑内障を予防するために散瞳薬点眼(例:トロピカミド・フェニレフリン塩酸塩点眼液を1日1~8回)を併用します6)。
▪後部ぶどう膜炎,汎ぶどう膜炎に対しては,アザチオプリンやシクロスポリンを併用します。アザチオプリンやシクロスポリンで再燃する場合や視力低下のおそれがある場合は,抗TNF-αモノクローナル抗体(インフリキシマブ,アダリムマブ)を投与します4)。抗TNF-αモノクローナル抗体は,アザチオプリンやシクロスポリンと併用することも可能です。
▪急性深部静脈血栓症に対しては,アザチオプリンやシクロスポリンを併用します。大静脈炎による血栓症を認める場合は,シクロホスファミドを考慮します。難治例では抗TNF-αモノクローナル抗体(インフリキシマブ)を考慮します4)。
▪肺動脈を含む動脈病変の場合は,シクロホスファミドを併用します。難治例では抗TNF-αモノクローナル抗体(インフリキシマブ)を考慮します4)。
▪軽症の消化管病変の場合は,5-ASA製剤(メサラジン,サラゾスルファピリジンなど)を併用します。中等症例ではアザチオプリンを併用します。重症例や難治例では,抗TNF-αモノクローナル抗体(インフリキシマブ,アダリムマブ)を併用します4,8)。
▪急性の脳実質病変,髄膜炎に対しては,アザチオプリンを併用します。症例数は少ないのですが,MMFの有効性を示す報告もあります11)。重症例や難治例では,抗TNF-αモノクローナル抗体(インフリキシマブ)を併用します。インフリキシマブ無効例に抗IL-6受容体モノクローナル抗体(トシリズマブ)が有効であった報告もあります12)。
▪慢性進行型神経ベーチェット病では認知症様症状,精神症状,体幹失調,構語障害が進行します。ステロイド,シクロホスファミド,アザチオプリン,コルヒチンは無効とされ,メトトレキサートが有効であるとされています。難治例ではインフリキシマブを検討します9)。
ピットフォール
➡後部ぶどう膜炎に対してステロイド単剤で治療をすることは推奨されません4)。ステロイド単剤では,減量過程で眼炎症発作が誘発されるからです。
➡静脈血栓症を生じた場合,肺動脈にも炎症があり肺動脈瘤を合併している場合があります。抗凝固療法は肺動脈瘤からの出血リスクを増大させるため,抗凝固薬を開始する前に必ず造影CT検査で肺動脈瘤の検索を行います。
➡動脈炎をコントロールしないで血管手術を行うことは,吻合部動脈瘤形成などの術後合併症が多くなり,死亡率が高くなることが指摘されています4)。血管手術の前後は免疫抑制療法にて動脈炎を十分に抑制する必要があります。
➡消化管病変は深掘れ潰瘍を形成することが多く,穿孔,大出血,閉塞など緊急手術となることもめずらしくありません。
➡神経病変に対しては,シクロスポリンは増悪因子であるとされます。活動性の神経病変がある場合だけでなく,非活動性の神経病変に対してもシクロスポリンは禁忌です4,9)。
7 寛解維持療法としてsteroid sparing agentは 何かあるか?
▪寛解導入療法として開始したコルヒチン,免疫抑制薬,抗TNF-αモノクローナル抗体は寛解維持療法としても継続します。
▪血管炎に対してシクロホスファミドを使用した場合は,長期投与による毒性が懸念されるため,アザチオプリンや抗TNF-αモノクローナル抗体による寛解維持を行います。
MEMO
ベーチェット病の寛解導入療法としてステロイドに併用されることの多いアザチオプリンですが,活性体が細胞内に蓄積するまで3カ月程度要するので即効性がありません(☞1章1)。投与時期は寛解導入期であったとしても,臨床効果は寛解維持期に出現すると考えられます。
本邦の「ベーチェット病眼病変診療ガイドライン」には,「(アザチオプリンは)海外ではベーチェット病に対してよく使われている薬剤であり,1990年には二重盲検試験により有効性が示された13)。(中略)しかし,本邦では従来の治療経験からは著効を示す有用な薬剤とは考えられていない」と明記されており,推奨薬からは外れています6)。
一方で,2018年に欧州リウマチ学会から発表されたリコメンデーションには,眼病変に対してアザチオプリン「推奨度A」と記載されています4)。この本邦と欧州での推奨度の乖離には,アザチオプリンに寛解導入効果を期待するか,寛解維持効果を期待するかの違いが現れているように思われます。
8 ステロイド減量のスピードは?
▪発熱などの全身症状のみで主要臓器病変がない場合は,初期用量を1~2週継続し,1~2カ月以内を目処にPSL 10mg/日に減量します。
▪主要臓器病変がある場合は,初期用量を2~4週継続し,2~4カ月以内を目処にPSL 10mg/日に減量します。
▪PSL 10mg/日以降は,毎月1mg/日ずつ寛解維持可能な最小限の用量(通常PSL 5mg/日以下)まで減量します。
9 減量は何を指標にすればよいか?
▪ステロイドを開始する根拠となった発熱などの全身症状や主要臓器病変が寛解状態にあることを確認しながら減量します。寛解状態になると通常CRPは陰性化するので,CRPの推移を参考にします。
▪ステロイド減量中に粘膜皮膚病変が再燃することがありますが,粘膜皮膚病変は全身ステロイド療法の適応にはならないので,よほど重症でない限りステロイド減量の妨げにならないことがほとんどです。
10 ステロイドは中止できるか?投与期間は?
▪発熱などの全身症状のみで主要臓器病変がない場合は,半年~1年以内にステロイドを中止できることが多いです。
▪髄膜炎も主要臓器病変の中ではステロイドを中止しやすい病変です。1~2年以内にステロイドを中止することが期待できます。
▪髄膜炎以外の主要臓器病変でもステロイドを中止できることはありますが,再燃を繰り返す症例ではPSL 10mg/日以下(通常PSL 5mg/日以下)の寛解維持量を数年以上にわたり継続することもあります。最近では,抗TNF-αモノクローナル抗体によりステロイドを中止できる症例も増えてきています。
ピットフォール
➡ベーチェット病(欧米では「ベーチェット症候群」)の一部は,trisomy 8を伴う骨髄異形成症候群を基礎疾患として有しています。
➡trisomy 8によるベーチェット病の場合,消化管病変を合併しやすく,腸管ベーチェット病と診断されることが多いです。一方で,眼病変は少ないことが指摘されています。消化管病変のほかに高熱,血球減少症を起こしやすい特徴があります14)。
➡ベーチェット病に血球減少症,MCV高値,単球分画高値などの異常がある場合は,骨髄穿刺を施行したほうがよいでしょう。
➡trisomy 8によるベーチェット病の場合,ステロイド,免疫抑制薬,TNF阻害薬に治療抵抗性を示すことが少なくなく,骨髄異形成症候群に対してアザシチジンを投与することでベーチェット病に対する寛解導入が可能となることがあります15,16)。
11 モデル症例
症例:以前より口腔粘膜の再発性アフタ性潰瘍を認め,2週間前から発熱(45歳男性)
①口腔粘膜の再発性アフタ性潰瘍,陰部潰瘍,両下腿浮腫,表在性血栓性静脈炎,両下腿結節性紅斑,両膝関節炎が出現し,ベーチェット病と診断した。HLA-B51は陽性であった。
⬇
②表在性血栓性静脈炎だけではなく,深部静脈血栓症を認め,ベーチェット病による静脈炎(血管病変)を合併していると判断した。造影CT検査にて肺動脈瘤,肺塞栓症,大動脈病変の検索を行ったが,これらを疑う所見はなかった。
⬇
③PSL 60mg/日,アザチオプリン50mg/日,コルヒチン1mg/日による治療を開始した。PSL 60mg/日を2週継続し,4週後に血球減少症,肝障害がないことを確認してアザチオプリン100mg/日に増量した。
⬇
④ベーチェット病による症状がなく,炎症反応が陰性であることを確認しながら,PSLは30mg/日まで1週ごとに10mg/日ずつ,20mg/日まで2週ごとに5mg/日ずつ,10mg/日まで4週ごとに5mg/日ずつ減量し,治療開始16週後にはPSL 10mg/日まで減量した。以後,4週ごとにPSL 1mg/日ずつ減量を行い,治療開始36週後にPSL 5mg/日まで減量した。
⬇
⑤以後,アザチオプリンとコルヒチンを併用しながら3カ月ごとにPSL 1mg/日ずつ減量を行い,治療開始2年後にPSLを中止した。
文 献
(岩波慶一)
































