お知らせ
[緊急寄稿]「新型コロナウイルス感染症(COVID-19)診療の手引き」に対する意見書─移植感染症学の視点からみたCOVID-19[第2章]


たかはし こうた●1948年生。新潟大学医学部卒業後,東京女子医科大学を経て95年,新潟大学医学部泌尿器科教授。2010年新潟大学医歯学総合病院総括副院長,日本臨床腎移植学会理事長,日本臓器移植ネットワーク理事などを歴任,ABO血液型不適合腎移植を日本で初めて成功,2012年度日本医師会医学賞,文部科学大臣2014年度科学技術賞を受賞した

Point
「新型コロナウイルス感染症(COVID-19)診療の手引き 第5.1版」について率直な意見を述べた
ウイルス感染症は細菌感染症の既成概念が当てはまらない。患者の重症度に応じて病原体数をみれば明らかとなる
COVID-19は臨床経過と患者のウイルス量から4期に分類することができる。第1期のウイルス感染から始まり,重症化して第4期の免疫介在性炎症性間質性肺炎に変貌する
はじめに
ワクチン接種が,新型コロナウイルス感染症(COVID-19)のパンデミックを終焉させる最大の武器であることは誰でも知っている。それでもコロナウイルス感染症やサイトメガロウイルス(cytomegalovirus:CMV)感染症は,天然痘のようにこの世から撲滅することはできない。そこで第1章(WEB医事新報のみで掲載)では,COVID-19の予知診断ができた時点で,早期に抗ウイルス薬を投与することが,患者本人の治療はもとより,結果的に感染源を縮小させ,ひいては感染の拡大を防ぎ,流行を終息させることを述べた。
さらに胸部CT所見ですりガラス陰影を早期に発見し,間質性肺炎の診断をした時点で,宿主の生体(免疫)防御機能が高まったと察知し,それを抑えるために速やかに免疫抑制薬や抗炎症薬を投与することが重症化を防ぎ,寛解につながることを強調した。
第2章の本稿では,厚生労働省の「新型コロナウイルス感染症(COVID-19)診療の手引き」(第5.1版)1)について筆者が気づいたいくつかの問題点について意見を述べたい。
1. 厚生労働省「COVID-19診療の手引き」に対する率直な意見
この「手引き」1)は,全体的によく書かれているが,次の改定版を作成するに当たり,筆者がこれから指摘することについて,再考していただきたい。以下,厳しい批判とも取られるかもしれないが,そうではなく,筆者の率直な意見として耳を傾けてほしい。それによってCOVID-19患者の症状の軽減と救命率が向上すれば,結果的に患者の福音となる。
まず総論として,この「手引き」に沿ってCOVID-19患者を治療しても,あくまでも対症療法に過ぎないので,その効果はある一定基準まで到達するが,それ以上の効果は期待できない。したがって,救命率も予想したほど上がらないのではないかと懸念する。
それではこの「手引き」のどこに問題があるのか,筆者は考えてみた。枝葉末節のことはどうでもよいが,まずその本質について検討した。
治療効果が予想したほど上がらない主な原因は,昔から伝えられてきた感染症の既成概念にとらわれて,COVID-19の「急速に移り行く一連の病態」を把握していないからである2)~8)。したがって,重症化する新型コロナウイルス(SARS-CoV-2)間質性肺炎の本態も見抜けないので,発症メカニズムついても曖昧な表現となっている。当然,その曖昧さに基づいて治療法を考えるので,対症療法に過ぎず,それを補足するために「重症度分類とマネジメント」を付け加えている。この分類はそれなりに使い道があるが,あくまでも対症療法に過ぎず,読者を十分に納得させるに至っていない。改定した版でも形式的に変異株の特徴と自宅療養者の診療プロトコール(ダイジェスト版)が追加されたに過ぎない。エビデンスばかり唱えて,なぜ間質性肺炎にステイロド薬が効くのか,そのメカニズムについて何ら触れていない。
「手引き」の表題が「新型コロナウイルス感染症(COVID-19)診療の手引き」と書いてあるにもかかわらず,肝心な「患者のウイルス(量)」について書かれている箇所が少ない。「重症度分類とマネジメント」の項目に至っては12ページに渡ってページを割いているが,患者のウイルス(量)に関してほとんど記載されていない。
この重症度分類に筆者が推定した患者のおおよそのウイルス量を書き加えてみると,意外な真実が浮き彫りとなり,今までの感染症の既成概念では矛盾を感じ説明できないことに気づく(図1,表1)2)~8)。
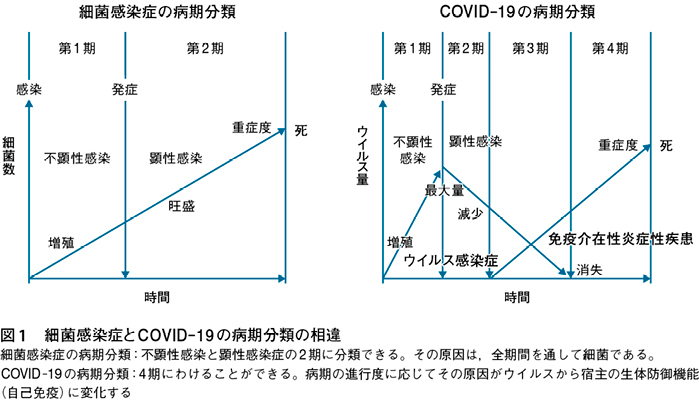
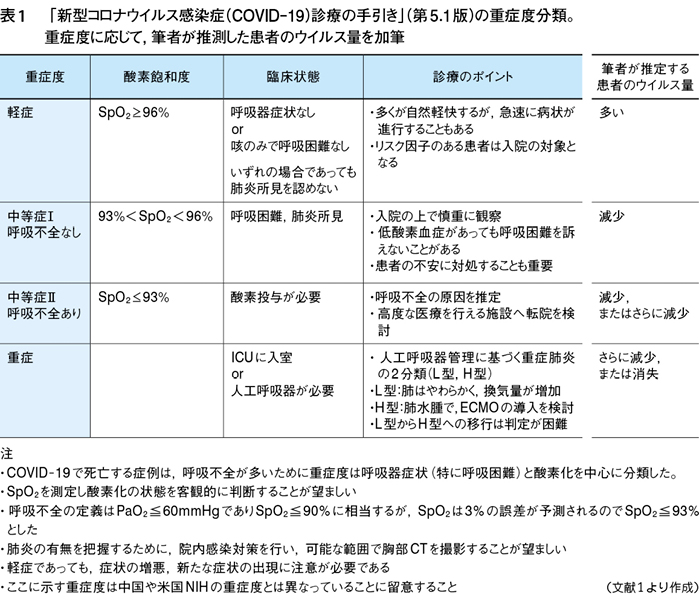
その既成概念とは,たとえば,細菌による感染症においては,一般にその病原体数の増加に伴い病巣が拡大して患者の病状が悪化し,患者の重症度が増す。ところが,ウイルス疾患において,特にこのSARS-CoV-2がもたらすCOVID-19においては,この概念が当てはまらず,患者のウイルス量が減少・消失しているにもかかわらず,重症度が増している。つまり,逆相関して,病状とウイルス量に乖離がみられる(図1)2)3)5)8)。この「手引き」は,ウイルス感染症を細菌感染症と同様に扱って,細菌感染症を基本に書かれているので,その矛盾点を解くことはできない。そもそもウイルス感染症は,細菌感染症とまったく異なる疾患であることを理解しておくべきである。
この病態を移植感染症学の視点から説明すると,今まで繰り返し述べてきたが,COVID- 19で特に重症化する例では,一言で言えば「急速に移り行く一連の病態」,すなわち,単なるウイルス感染症から宿主における生体(免疫)防御機能の急激で異常な高まりにより,おのれ自身の肺組織に障害を与える免疫介在性炎症性疾患に変貌しているからである2)~8)。
また,厚生労働省の「手引き」に戻るが,重症度分類(表1)の注釈に「COVID-19で死亡する症例は,呼吸不全が多いために重症度は呼吸器症状(特に呼吸器困難)と酸素化を中心に分類」という視点から書かれたと説明されている。そうであれば,この「重症度分類とマネジメント」は患者の初診や救急外来時のトリアージとしての治療には大いに活用される。しかし,「新型コロナウイルス感染症の診療の手引き」と謳っている以上,COVID-19の一連の臨床経過に沿って,患者のウイルス量と対峙しながら,筆者が作成した図1のような進行度分類も付け加えることを提案する。
COVID-19の治療は,基本的にウイルスに対する治療と免疫能が高まった患者に対する治療の両面作戦が必須であるので,患者のウイルス量の記載がないのでは治療戦略が立てられない。
筆者の作成したウイルス量の推移と生体防御機能の程度によって規定される病態を考慮した進行度分類を参考にすれば,治療方針が立てやすくなり,根治的治療につながる。ひいては治療効果が向上し,救命率も高くなる(図1)3)6)8)。
さらにこの「手引き」において,患者のウイルス量について書かれている箇所を検討してみよう。
2. 第1の指摘:ウイルス量と急性免疫介在性炎症(自己免疫)
ウイルス量の記載について,「手引書」の「2 伝播様式」(p7)の項で,「潜伏期・感染可能期間」には,こう書かれている。
【潜伏期・感染可能期間】
潜伏期は1~14日間であり,曝露から5日程度で発症することが多い(WHO)。発症前から感染性があり,発症から間もない時期の感染性が高いことが市中感染の原因となっており,SARSやMERSと異なる特徴である。
SARS-CoV-2は上気道と下気道で増殖していると考えられ,重症例ではウイルス量が多く,排泄期間も長い傾向にある。
「2 伝播様式【潜伏期・感染可能期間】」(p7)より
まず,「重症例ではウイルス量が多く,排泄期間も長い傾向にある」とあるが,この「重症例」とはどのような病態を指しているのか。呼吸器不全,すなわち重篤な間質性肺炎を指しているのか。さらに,「ウイルス量が多く,排泄期間も長い傾向」という根拠に,どれくらいの文献数があるのか,また,どの文献を引用したのか教えていただきたい。「傾向」という言葉で逃げないでほしい。
前に述べたように,筆者は,重症化する要因はただ短絡的にウイルス量が多いばかりとは考えていない。重症化はウイルスの抗原性と,それに対する宿主における生体防御機能の程度との相互関係により決まる(図2)2)~8)11)。
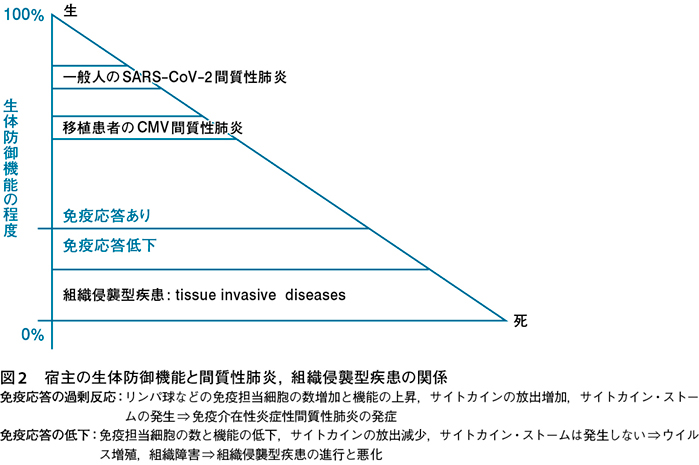
重症化するウイルス性間質性肺炎は,何もSARS-CoV-2間質性肺炎が初めてではなく,その発症メカニズムは,既に約40年前,1987年にGrundyらがLancetに,その後,宮崎医科大学の副学長で微生物学講座教授の南嶋洋一や筆者によってCMV間質性肺炎で明らかにしている9)〜11)。
Grundyらは動物実験モデルを駆使し、間質性肺炎の発症はウイルス感染が引き金となっているが、ウイルス量とは必ずしも相関せず、その発症時には、ときにウイルスが消退していることもあると報告している9)。また,南嶋は筆者が編集した書籍「臓器移植におけるサイトメガロウイルス感染症」の中で,Grundyらの間質性肺炎の発症メカニズムついて,“同種骨髄移植後のCMV間質性肺炎はCMVに感染した肺細胞の表面に発現したウイルス抗原を,Tリンパ球が認識して反応することによって成立する免疫病である”との説を紹介している11)。
我々も腎移植後,CMVやPneumocystis jiroveciiによって引き起こされる悲惨な間質性肺炎を多く体験し,その治療に当たり,その経験と成績を本稿の参考文献に載せた通り,たびたび報告してきた11)~27)。
また,最近,今井らはハムスターを用いたSARS-CoV-2の感染モデルで,ヒトの間質性肺炎に類似した重い肺炎症状の病態を作成できたことを報告している28)。
したがって,これらの既知のデータを総合して考えれば,SARS-CoV-2間質性肺炎は,ウイルスが起因となって高まった免疫により発症する急性免疫介在性炎症性疾患が本態である2)~7)。
この間質性肺炎は,宿主の免疫能が著しく低下しているときに発症するのではなく,ウイルスという抗原に対して,まだ免疫応答のできる程度の生体防御機能が温存された宿主に発症する(図2)。
さらに詳しく述べれば,免疫担当細胞が免疫応答できる十分な免疫能が温存された宿主では,ウイルスに暴露された肺の感染肺胞Ⅱ型上皮細胞を修復するために,免疫担当細胞,特にTリンパ球が動員され,過剰に活性化される。それに伴い炎症性サイトカインが多く放出され,サイトカイン・ストームが発生する。やがてその結果として,ウイルスの増殖は抑制され,ウイルス疾患としては回復に向かう。しかし,活性化された免疫担当細胞の働きはそれにとどまらず,暴走して自己の肺組織を損傷し,間質性肺炎へと病態が進む。繰り返しになるが,この肺炎を一言で言うと,免疫介在性炎症性間質性肺炎(immune-mediated inflammatory interstitial pneumonitis)であり,さらに細胞性免疫からみればT細胞関連型炎症性間質性肺炎(T cell-mediated inflammatory interstitial pneumonitis)である2)〜8)11)。
すなわち,この間質性肺炎は,ウイルスの抗原性とそれを迎え打つ宿主の生体(免疫)防御機能の相対的な関係が,ある閾値に達し一致したときに発症する免疫介在性炎症性疾患の一種である。したがって,その病巣は,免疫反応が主体であるので,急速に拡大し,病状は悪化を辿る。一方,治療が奏功すれば速やかに患者は回復する。
以上のことから,間質性肺炎が発症する,この一瞬の時期がきわめて重要で,このときに副腎皮質ステロイド薬などの免疫抑制作用,抗炎症作用のある薬剤の投与の有無が,患者の予後を左右する鍵となる。
現場で直接COVID-19患者の治療に当たっている医師らにとって,この一瞬の時期に,ステロイドを投与することがウイルスの増殖を助長するのではないかという懸念が頭に浮かび,ステロイド投与になかなか踏み切れないことがある。筆者も移植後のCMV間質性肺炎を経験した初期の頃に同様の体験をした。
しかし,患者のウイルス量は感染症発症時に一番多い29)。そして免疫担当細胞の働きによりサイトカイン・ストームが発生して,間質性肺炎が発症したときにはウイルス量は増加するのではなく,その結果,逆に減少,または消失している。その証しとして,この時点で症例によってはしばしばウイルス検査が陰性化している。したがって,ステロイド療法の適応の妨げにはならない2)3)6)7)。
次のような報告例もこの間質性肺炎を理解するための参考となる。
横浜市立大学の山中グループは,2020年2月以降にSARS-CoV-2に感染し,その後寛解した376名の患者における半年後の中和抗体保有率を調べた。その結果,COVID-19重症度分類で,不顕性感染と軽症患者を合わせた群では97%,中等症と重症患者を合わせた群では100%であった。さらに症状が重いほど強く残る傾向があったことをテレビや新聞などのマスメディアに発表している。
ほとんどの人はこの97%と100%の数字,わずか3%の差しかないので,これら2群は同等と考えるが,この差には大きな意義がある。
このデータが示していることは,免疫能が低下しているから間質性肺炎が重篤化すると一般の人々が考えることとは裏腹に,重篤な間質性肺炎を経験した患者ほど軽症間質性肺炎患者に比べて,むしろ免疫能が相対的に高く,罹患中に激しい抗原抗体反応(炎症)が起きていたことを証拠として残した痕跡である。その結果,抗体保有率や抗体価も高くなり,その保有期間も長くなった傾向がみられる2)。
なお,生体防御機能が著しく低下した宿主では,免疫担当細胞の数は減少し,機能も落ちているので,ウイルスの侵入にはほとんど反応できず,ウイルスが直接に組織に浸潤し,破壊する組織侵襲型疾患(tissue invasive diseases)の形を取る(図2)。したがって,サイトカインの放出も少なく,「サイトカイン・ストーム⇒間質性肺炎」の一連のパターンは取らない。やがて静かな死を迎える2)6)。
逆に間質性肺炎を発症する宿主は,免疫能がまだ十分残っているので,一時的に高まった免疫能をステロイドのような免疫抑制・抗炎症性効果のある薬剤で制御し,その後,徐々に免疫能を高めれば治癒する可能性がある2)6)11)。
3. 第2の指摘:ウイルス検査法の意義
続いて,次の課題を指摘したい。「病原体遺伝子の検出」について,2カ所引用する。
【潜伏期・感染可能期間】
~中略~ 発症から3~4週間,病原体遺伝子が検出されることはまれでない。ただし,病原体遺伝子が検出されることと感染性があることは同義ではない。感染可能期間は発症2日前から発症後7~10日間程度と考えられている。なお,血液,尿,便から感染性のあるSARS-CoV-2が検出されることはまれである。
「2 伝播様式【潜伏期・感染可能期間】」(p7)より
【COVID-19のウイルス排出期間】
遺伝子は長期間検出するものの,感染力があるウイルス排出期間は10日以内
「インフルエンザとCOVID-19の相違」(表 3-6,p28)
潜伏期・感染可能期間の箇所に,「発症から3~4週間,病原体遺伝子が検出されることはまれでない。ただし,病原体遺伝子が検出されることと感染性があることは同義ではない」とあり,また,ウイルス排出期間のCOVID-19の箇所に,「遺伝子は長期間検出するものの,感染力があるウイルス排出期間は10日以内」と書かれている。
これらの意味不明な歯切れの悪い文章を書かれたメンバーは,かなり議論を尽くし,苦渋な選択をし,このような表現になったと思う。この表現からは,その趣旨のニュアンスは読者におおよそ伝わってくるが,どれくらいの読者に理解してもらえるか疑問である。すなわち,その責任を読者の解釈や判断に一任させている。
筆者個人の翻訳(解釈)では,この「病原体遺伝子を検出検査」とは核酸検出検査のPCR検査などを指していると思われる。PCR検査は感度が良いので,診断には向いているが,治療効果をみるためには,この精度の良さが逆に不利になる。すなわち,生きているウイルスはもちろんのこと活性のないウイルスの死骸もカウントしてしまう。生きたウイルスは感染力があるが,死んだウイルスには感染力がないということを言いたいと推測する。もう少し簡単にわかりやすく補足説明したほうが読者は理解しやすい。
筆者が,「新型コロナウイルス感染症(COVID-19)診療の手引き」を作成している委員会のメンバーに伝えたいことは以上である。
終わりに
筆者は,日本臨床腎移植学会の理事長の就任期間に,初めての腎移植のガイドラインの作成に携わったので,その作成が難しいことを十分に理解しているつもりである。したがって,私の提言を,この「手引き」を作成したメンバーを決して非難していると取らないで,あくまで意見として捉えてほしい。そしてさらに良い「手引き」の作成を願っている。筆者は,それによりCOVID-19患者の症状の軽減と救命率の向上に結びつけば素晴らしいと考えている。
【文献】
1) 厚生労働省:新型コロナウイルス感染症(COVID-19)診療の手引き, 第5.1版, 2021年7月5日.
[https://www.mhlw.go.jp/content/000801626.pdf]
2) 高橋公太:腎と透析. 2021;90(2):289-301.
3) 高橋公太:医事新報. 2021;5064:26-32.
4) 高橋公太:医事新報. 2021;5050:72.
5) 高橋公太:医事新報. 2021;5053;54.
6) 高橋公太:医事新報. 2021;5055:65.
7) 高橋公太:新型コロナによる肺炎は移植患者の感染症に酷似, 論座(朝日新聞), 2021.
[https://webronza.asahi.com/science/articles/2021022200005.html]
8) 高橋公太:腎と透析. 2020;89(4):735-43.
9) Grundy JE, et al:Lancet 1987;2(8566):996-9.
10) 南嶋洋一:臨床とウイルス. 1990;18(1):30-4.
11) 高橋公太, 編:臓器移植におけるサイトメガロウイルス感染症. 日本医学館, 1997.
12) Hill RB, et al:N Engl J Med. 1964;271:1021-7.
13) Takahashi K, et al:Herpes Viruses and Virus Chemotherapy. Kondo H, Ed. Excerpta Medica, 1984, p297-98.
14) 高橋公太:外科領域感染症. 酒井克治, 編. 医薬ジャーナル社. 1986, p249-73.
15) 高橋公太, 他:移植. 1986;20(Suppl):490-500.
16) 高橋公太, 他:日泌尿会誌. 1986;77:1188-99.
17) 高橋公太:抗生物質から化学療法の領域. 1986;2:202-10.
18) 高橋公太, 他:今日の移植. 1992;5:287-91.
19) Takahashi K, et al:Transplant Proc. 1978;19(5):4089-95.
20) Takahashi K, et al:Transplant Proc. 1989;21(1 Pt 2):1563-6.
21) 高橋公太, 他:日泌尿会誌. 1989;80:175-84.
22) Takahashi K, et al:Transplant Int. 1991;5(Suppl):133-7.
23) 八木澤 隆, 他:移植. 1992;27:586-93.
24) 高橋公太, 他:腎と透析. 1993;34:231-7.
25) Takahashi K:ABO-incompatible kidney transplantation. Elsevier, 2001.
26) 日本臨床腎移植学会:腎移植後サイトメガロウイルス感染症の診療ガイドライン2011. 日本医学館, 2011.
27) 高橋公太:日本臨床腎移植学会50周年記念誌. 日本臨床腎移植学会, 2017, p20-5.
28) 今井正樹, 他:日内雑誌. 2020;109(11):2260-3.
29) To KK, et al:Lancet Infect Dis. 2020;20(5):565-74.














































