お知らせ
■NEWS 新型コロナ抗原検査キット、患者発生数多い地域から供給─厚労省がガイドライン

厚生労働省は5月13日、新型コロナウイルス感染症(COVID-19)の診断に用いる国内初の抗原検査キット「エスプライン SARS-CoV-2」について、「患者発生数の多い都道府県における帰国者・接触者外来(地域・外来検査センターを含む)」と「全国の特定機能病院」から供給を開始するなどとしたガイドラインを策定、全国に通知した。

抗原検査キット「エスプライン SARS-CoV-2」(富士レビオ提供)
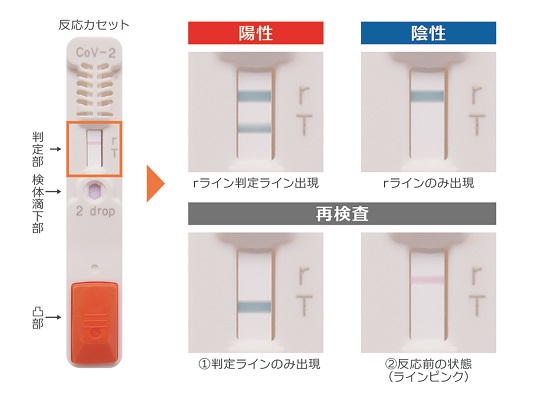
「エスプライン SARS-CoV-2」は富士レビオが4月27日に承認申請。5月13日に薬事承認され、同日の中医協で新型コロナウイルス抗原検出の保険適用(600点)も承認された。鼻咽頭ぬぐい液中のSARS-CoV-2抗原を迅速・簡便に検出するキットで、30分以内(陽性判定:約10~30分、陰性判定:30分)に検査結果を得られることから医療現場の期待は大きい。
ただ、同キットは、陽性となった場合は確定診断とすることができるものの、除外診断には適さず、陰性の場合、確定診断のためには医師の判断でPCR検査を行う必要があるとされている。また、当面供給量も限られることから、厚労省はガイドラインで、患者発生数の多い地域やPCR検査を実施できる医療機関を中心に供給対象を順次拡大していく方針を示した。
「無症状者への使用は推奨されない」
ガイドラインは、キットの用途・使用方法も規定。「医師が、新型コロナウイルス感染症を疑う症状があると判断した者に対して、必要性を認めた時に使用する」とし、「無症状者への使用は、現段階では推奨されない」と明記している。
厚労省は、今後クラスターが発生した医療機関・施設に対して積極調査を行う際にも同キットを活用する意向だ。
中医協・診療側委員「現場に早く回してほしい」
オンラインで行われた13日の中医協では、診療側委員から「供給量がまだ十分ではないということだが、クラスター発生を防止するために、帰国者・接触者外来を持たない医療機関や介護施設の現場に早く回してほしい」などの意見が出された。
現段階の生産体制について富士レビオは「週20万テストの生産体制を構築している」としている。
【関連情報】
厚生労働省新型コロナウイルス感染症対策本部「SARS-CoV-2 抗原検出用キットの活用に関するガイドライン」(5月13日)















































