お知らせ
[緊急寄稿]新型コロナウイルス間質性肺炎の検証─初発と再発では,なぜ発症メカニズムが大きく変わるのか(高橋公太)

2. 考察
(1)SARS-CoV-2間質性肺炎の初発と再発・再燃の比較と相違
これまで筆者は,健常者,透析患者,および腎移植患者のSARS-CoV-2間質性肺炎の診療を経験してきたが,その本質に違いはあまりない。表1はSARS-CoV-2間質性肺炎の初発時と再発・再燃時を比較したものである。これらの所見から,SARS-CoV-2は宿主に抗原として働き,宿主は,初発では自然免疫,すなわち免疫の一次応答として反撃し,再発・再燃では獲得免疫,二次応答として反撃している。


①初発時におけるSARS-CoV-2間質性肺炎
COVID-19はSARS-CoV-2による急性ウイルス感染症として始まる。ACE2受容体が標的受容体で,ここに接着,侵入して細胞内で増殖する。
ACE2受容体は鼻腔,咽頭,喉頭の上気道粘膜に多く存在するので,初発時の感染経路は,上気道から始まり,やがて下気道から肺へと広がり,呼吸器感染症となる。そのため気道の炎症,浮腫を招き,上気道の激しい疼痛,咳嗽および嗄声などの症状を引き起こす。重症例では,声門浮腫,気道閉塞を伴う。さらに病変が気管,気管支,肺胞に及べば呼吸困難となる3)〜6)。
肺においては,ACE2受容体は肺胞Ⅱ型上皮細胞に発現しているので,この細胞が障害されると含気性を保つ表面活性物質(サーファクタント)の産生が障害され,肺嚢胞が虚脱し,呼吸機能不全を招き,間質性肺炎が発症する。これが胸部CT所見や胸部X線所見ですりガラス状陰影として反映される16)。
さらにサイトカイン・ストームにより肺胞の基底膜の透過性が増して,滲出液が漏出して,肺胞に硝子膜を形成するので,酸素/二酸化炭素のガス交換が阻害され,呼吸不全を起こし,患者は息苦しさ訴え,さらに進行すれば呼吸困難となる3)〜6)。
「PCR検査陽性」「血中酸素飽和度の低下」「胸部CT所見でのすりガラス状陰影」の3徴候(トリアス)がそろえば,SARS-CoV-2間質性肺炎の確定診断となる。早期に適切なステロイド投与をすれば,速やかに改善する3)〜6)17)。
この時期には一般に患者のウイルス量は減少,消失しているが,免疫応答が弱い免疫不全患者や高齢者では抗SARS-CoV-2薬とステロイドの両薬剤を同時に投与することも念頭に置く18)。
間質性肺炎の臨床的特徴は,強い炎症のわりに胸水は少なく,聴診所見では,肺水腫のときによく聞かれるような水泡性ラ音などのラ音はほとんど聴取されない。
②再発・再燃時におけるSARS-CoV-2間質性肺炎
再発・再燃例は,患者の体内に残存していたSARS-CoV-2が増殖して肺に障害をもたらしていると思っている人が相変わらず多い。そのような症例はよほど生体防御機能が低下し,免疫の一次応答,二次応答もなく,したがってサイトカイン・ストームも発生しない易感染性宿主で,免疫応答が弱い例外である。
一般に再発・再燃例ではSARS-CoV-2検査陰性,すなわち,患者の体内からもはやウイルスは消失している。上気道の疼痛はなく,気道閉塞も伴わず,突然,咳嗽と息切れで発症する。さらに肺病変が急速に広がり,酸素/二酸化炭素のガス交換ができなくなり,呼吸困難となる。初発時の間質性肺炎よりも,重症度が急速に進行するので注意が必要である。
再発・再燃例を振り返ってみると,初発時の病期分類が前期(ウイルス期)から後期の急性免疫疾患期に進行しており,その治療としてステロイドの投与開始が遅かったり,投与量が不十分であった例である。
これらの患者では肺組織に浸潤したリンパ球を十分に抑制できず,感作されたリンパ球がメモリー・セルとして生き残り,やがて,クラススイッチされたメモリー・セルが何らかの刺激により,または何らかの刺激がなくとも時間の経過とともに増殖し,ある一定量に達したとき,再びサイトカイン・ストームが発生し,免疫介在性炎症性反応が再燃,または再発する7)19)。
肺胞における病巣の拡大は免疫の二次応答であるため,加速度的に進行する。このような免疫介在性炎症性反応は,初発からかなり時間が経過しているので,組織に浸潤している細胞は未熟なTリンパ球から成熟Tリンパ球に置き換わっており,さらにBリンパ球や形質細胞なども加わって,ステロイドに抵抗性を示すため,高用量のステロイド・パルス療法が必要となる1)。
Bリンパ球や形質細胞を抑制するためには,非特異的免疫抑制薬やモノクローナル抗体医薬品が必要になるかもしれない。ここで十分な治療を施さないと,骨髄移植や輸血による移植片対宿主病,臓器移植の急性拒絶反応などと同じく,COVID-19の後遺症(Long COVID)として慢性免疫疾患となり,慢性臓器不全となる2)。
本来,我々が持っている免疫機構は感染症を治すことを目的に機能するが,重症例では,それを通り越して自己の組織に障害を与える免疫疾患に変貌する。すなわち,サイトカイン・ストームの発生は「諸刃の剣」で,一方ではウイルスの増殖を抑制,消滅させるが,他方では,患者自身の組織に障害を与える自傷行為となる。
しかし,考え方を変えてみれば,免疫応答があるということは,宿主にとって回復できるチャンスであり,この「嵐」を制御できれば病状は速やかに回復する。
間質性肺炎に代表される免疫疾患の病態は,広義の自己免疫疾患(autoimmune disease)である。また,細胞性免疫からみれば,その主体はT細胞関連型炎症性疾患であり,自己(auto)抗原と同種(allo)抗原の違いはあるものの,臓器移植の急性拒絶反応と類似した免疫介在性炎症性反応である。
③ウイルス組織侵襲型疾患
生体防御機能が著しく低下した易感染性宿主患者では,感染を受けても免疫応答が弱いので,免疫の一次応答,二次応答もなく,サイトカイン・ストームが起こらない。一見,症状は乏しいが,ウイルスが体内で長くとどまり,異常増殖してウイルスが直接組織を侵食する組織侵襲型疾患を引き起こす。そのような状態では,腸管でも防御機能の壁が崩壊し,bacterial translocation(素通り現象)が起きて腸内細菌が血中に入り,敗血症を起こして,やがて患者は死を迎える3)〜5)。しかし,このような症例はきわめて限定されているので,それほど心配する必要はない。
④適切なステロイド治療
(a)ステロイドの効果
ステロイドのデキサメタゾンは,COVID-19治療薬として,保険適用されている。コルチコイドの糖質作用として最も力価が高いステロイドの一つである。しかし,リンパ球を抑制することを第1の目的とすれば,1日の投与量が6mgでは十分とはいえない。
主なステロイドのコルチコイドの糖質作用効果は,プレドニン:メチルプレドニゾロン(MP):デキサメタゾン=4:5:25とされている。
腎移植の急性拒絶反応では,従来からMPが使用されてきた。初回投与量は500~1000mg/日で,その後,漸減することが多い。SARS-CoV-2間質性肺炎は,臓器移植における急性拒絶反応と同様の反応と考えられるので,現在,保険適用で認められているデキサメタゾン(6mg/日10日間)の投与量は少ない2)14)20)。
不十分,不適切なステロイド療法は対症療法にすぎず,一過性の症状の軽減にはつながるが,リンパ球が十分に抑制されていないので,根治的治療にはならない。かえって,ステロイド抵抗性感作リンパ球がメモリー・セルとして生き残り,急速に異常増殖し,間質性肺炎が再発,再燃する原因となってしまう。これは免疫の二次応答であるため,加速度的に病巣が拡大し,難治性となり,患者の生命を脅かす結果となる。
(b)ステロイドの副作用,合併症
ステロイドは,その効果が優れているため,初めて合成されてから70年以上も経過した現在でも臨床の場で多用されている。しかし,副作用,有害事象が多い薬剤でもある。その使用量の安全域を考え,深追いせず,ステロイド抵抗性の病態に対しては他の免疫抑制薬を積極的に使用することも考慮する。
なお,今回提示した2症例とも原疾患が糖尿病で,糖尿病性腎症を経て末期腎不全となり,腎移植を受けた。以後,免疫抑制療法のため,低用量のステロイドが投与されている。さらに間質性肺炎の治療のため,その投与量を増量したので,患者の耐糖能が悪化すると考え,厳重なインスリン強化療法を実施し,副作用や有害事象の合併症防止に努めている。
⑤人工呼吸器やECMOの適応
呼吸不全で,人工呼吸器や体外式膜型人工肺(extracorporeal membrane oxygenation:ECMO)の適応患者の予後は,以前に比べて改善したとはいえ,開始したときの重症度と施設間で差が見られ,離脱できたとしても長期的に見れば決して楽観視できない。
離脱後,肺気腫,気管支拡張症などのLong COVIDに悩まされる患者が多い。さらに肺線維症が進行して,慢性呼吸不全となって肺移植の適応となった症例もある10)。
このような重篤な病状になる前に,これまで述べてきた治療を迅速に実施し,人工呼吸器やECMOの適応にならないように努力する。
(2)移植感染症学の応用と相対性感染症学の提唱
感染症の病態は,「病原体」と「宿主の生体防御機能」の相対性によって決まる。これまでの感染症の概念を考えてみると,「病原体が,健常人と呼ばれる生体防御機能の一定の範囲にいるヒトに侵入し,身体をむしばみ,発症させる疾患」を基準に考え,診断してきた。これがいわゆる感染症の既成概念におけるものさし・基準であり,我々はそれを当然のこととして受け止めてきた。
ところが臓器移植は,拒絶反応を抑制する目的のために生体防御機能を免疫抑制療法により人為的に低下させるため,新たな感染症の病態を発症させるに至った。
そして,免疫抑制療法の強さにより,個々の症例において生体防御機能の低下の範囲にバラツキができ,同じ病原体であってもその病態は,カメレオンの皮膚の色が周囲の環境によって変わるのと同じように,刻々と変わっていく。このような感染症を一般では日和見感染と呼んでいる。
これは,ある意味では人為的に作成した実証感染症(experimental infection)であり,見方によっては医原性感染症(iatrogenic infection)と呼ばれる。
移植感染症学はこうした感染症を研究する学問である。したがって,その予防や治療においては,病原体,宿主の生体防御機能,および薬剤の相互関係,すなわち,「相対性感染症学」を念頭に置きながら実施する。そしてこの感染症の概念を理解することが新興感染症,今回のCOVID-19の病態や予防・治療対策に大きく貢献する21)。
(3)世界的規模で同時に起きたCOVID-19流行初期の悲劇と今後の感染症の医学・医療の取り組み
①免疫抑制療法の機会を失った流行初期
COVID-19流行初期,救急の現場に重篤なSARS-CoV-2間質性肺炎に陥った患者が搬送されたとき,救急医は,その患者の胸部X線写真において,全肺野に及ぶ「すりガラス状陰影」を見た瞬間,細菌性肺炎や肺結核のイメージが脳裏に浮かび,「これは大変な肺炎だ」と第一印象を持ち,そしてこの画像所見はウイルスの異常増殖を反映していると判断し,「ステロイドの投与なんてとんでもない。ステロイドを投与すれば,さらにウイルスが増殖する」と考えたと思う。これが今までの感染症の既成概念である19)。
「すりガラス状陰影」所見は,いわば,暴風雨を起こした台風が去った後の爪痕である。すなわち,主役のウイルスがひそかに舞台から降りて,いつの間にかウイルスに洗脳された影武者,宿主自身の生体防御機能が主役として入れ替わっていることに,ほとんどの医療関係者は気づいていなかった12)13)。
このSARS-CoV-2は,まず直接障害として感冒様症状を引き起こす。そして患者の体内では,自然免疫の防御として免疫担当細胞からインターフェロンをはじめとするリンホカインが大量に放出されるサイトカイン・ストーム(嵐)が発生して,ウイルスの増殖を抑制し,消失させる。一方で,間接障害として,人類が経験したことのない異例の速さで間質性肺炎に代表される急性免疫疾患に変貌している。その結果,あまりにも急速に移りゆく病態の対応に,医師の固い頭脳はついていけず,病態が既に免疫疾患に移行しているにもかかわらず,舞台から降りたウイルスを追い求め,病原体の治療に専念した。その結果,免疫抑制療法という治療を実施すべき機会を失ってしまった。急性免疫疾患に移行した時点で,ステロイドを投与すれば,速やかに病状が回復したと思うと残念である13)。しかし,現場の医師がSARS-CoV-2間質性肺炎の発症メカニズムを理解できるまでかなり時間を要したため,世界的なパンデミックとなり,多くの犠牲を払った。
これまで繰り返し述べてきたように,間質性肺炎の発症メカニズムは意外と単純であり,その治療も一律で単純である19)21)。
同様のメカニズムで発症する移植患者のCMV間質性肺炎を経験した筆者が,この3年間,警鐘を鳴らし,その治療法を医学界に提唱し続けてきたが,その教訓が十分に生かされなかったのはきわめて遺憾である2)〜8)11)〜15)22)〜27)。
②医学教育に「相対性感染症学」を
症例1の腎移植患者は,抗SARS-CoV-2薬を一度も使用していないが,寛解させることができた。すなわち,従来の古典感染症の治療は,病原体に注目し,それとの闘いに重点が置かれていたが,COVID-19においては,ずれて狂った自己の生体防御機能をいかに正常に戻すか(「免疫抑制療法」というよりも「免疫調整療法」と言ったほうが適切かもしれない)ということに,第2の重点を置く必要がある。このことが今までの古典感染症の医療において大きく欠けていた盲点である19)21)。
今後も新興感染症が繰り返し流行することが懸念されるので,一般臨床医においても免疫抑制療法に精通しておくことが大切である。さらに卒前卒後の医学教育にも「移植感染症学」を特殊な学問とは捉えず,「相対性感染症学」として組み入れるべきである。
今回提示する症例をあえて腎移植患者にした理由は,腎移植患者における急性免疫疾患,特に間質性肺炎の治療には,移りゆく病態,組織に浸潤する細胞の分化の度合い,種類に応じて,それに適した免疫抑制薬の選択が必要になるからである。移植に携わる医師は日頃,薬剤の至適投与法(therapeutic drug monitoring:TDM)に基づいた免疫抑制薬の科学的投与法に精通している19)21)。
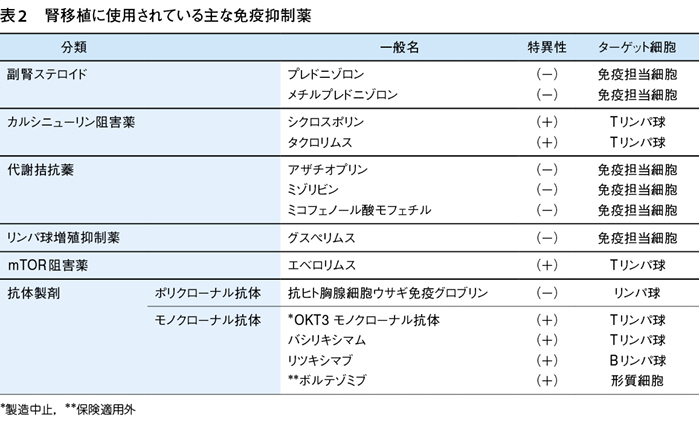
わが国では,腎移植患者には表2に示した免疫抑制薬が保険適用となっている1)。しかし,健常人にはこれらの多くは保険適用にならないので,現在,原則としてSARS-CoV-2間質性肺炎治療に応用できない。ここに保険診療の限界がある。
わが国の国民皆保険は素晴らしい制度で,今後も継続していく必要があるが,未知の疾患の治療には足枷になることもあるので,今後,その兼ね合いをどのようにするか解決しなければならない大きな課題である。
③若手医師へのメッセージ
最後に,約50年にわたり切磋琢磨してきた「団塊の世代」の一医師である筆者が,COVID-19の医療にも携わった経験から,将来の医学・医療を担う,まだ頭に柔軟性のある新進気鋭の若手医師にメッセージを送りたい。
重篤なSARS-CoV-2間質性肺炎により苦しんでいる患者を目の当たりにして,厚生労働省の新型コロナウイルス感染症(COVID-19)診療の手引きや各学会の感染症診療ガイドラインに沿って治療を開始しても患者の容態が一向に好転しない場合14),これまでの感染症の既成概念(古典感染症学)に疑問を抱き,その病態の発症メカニズムを考え直せば,感染症(感染症 ⇒ 免疫疾患)にも免疫抑制療法という有効な一手段があることに気づく。そしてこの治療法が決して奇想天外の治療でないことも自覚する。しかし,その後が問題である。この治療を自ら実行に移せるかどうかによって,患者の予後が決まってしまう。
言い方を変えれば,「医師の能力,技量,さらに裁量」が試される。頭の中で理論上,正しい治療であることは理解できても,これまで自分にとって経験したことのない治療であり,ガイドライン等と治療方針が異なるため,一瞬,躊躇する。
もし,実行に移した場合,その結果が患者の生命を逆に脅かすのではないか,そして,患者やその家族から訴えられるのではないか,権威や学会のガイドラインに逆らえば,自分の立場が悪くなるのではないかと,様々な葛藤が頭の中で渦巻き,錯綜し,一抹の不安を覚える。
さらに「医師の使命」とは何か,「医師の良心」とは何か,「医師の裁量」と何かと問いただしているうちに,患者の容態は刻々と深刻さを増していく。その時,主治医の「心」は揺れ,精神的な重圧となる。
それでは,この厳しい状況や重圧をどう跳ね返せばよいのか。それは日頃の「たゆまぬ努力」「患者への愛情」「多様性のある考え方や意見を取り入れる柔軟性と寛容さ,謙虚さ」「修練された経験」「幅広く深い知識に基づいた洞察力」,さらに磨き上げられた臨床医の「鋭い勘」を持って,確固たる治療方針を立てることである。それを実行に移せば,SARS-CoV-2間質性肺炎患者の病状は改善し,健康を取り戻すだろう。
そして,そのときに初めて主治医の「心」のなかに自然と達成感が芽生える。それが臨床の醍醐味と言っても過言ではない。その勇気ある前進の第一歩が,尊い命を助けることにつながり,臨床医にとっても明日への活力の源となる。
ステロイドは,どのような小さな医療機関でも常備薬として置いてあるので,決して言い逃れはできない。かくも臨床は患者の命がかかっているので,厳しいのである。
おわりに
腎移植患者に発症したSARS-CoV-2間質性肺炎の症例を提示し,初発と再発・再燃の間質性肺炎の発症メカニズムの相違とそれに基づく治療法について述べた。
資料の一部を提供して協力していただいた中東遠総合医療センター(静岡県)太田智陽医師, 白石病院(鹿児島県)白石幸三理事長,および南千住病院(東京都)蒲谷堯理事長に感謝の意を表する。
また,この3年間,筆者の論文,コラムに対するご助言と編集に携わっていただいた日本医事新報社編集局の永野拓紀子様に深謝を表する。
【利益相反】本論文に関連する利益相反(COI)はない。
【文献】
1) 高橋公太, 編:腎移植における免疫抑制療法. 日本医学館, 1998.
2) 高橋公太:医事新報. 2021;5083:38-46.
https://www.jmedj.co.jp/journal/paper/detail.php?id=17992
3) 高橋公太:Organ Biology. 2022;29:90-106.
4) 高橋公太:日臨腎移植会誌. 2021;9:44-56.
5) 高橋公太:腎と透析. 2020;89:735–43.
6) 高橋公太:医事新報. 2021;5064:26-32.
https://www.jmedj.co.jp/journal/paper/detail.php?id=16903
7) 高橋公太, 編:臓器移植におけるサイトメガロウイルス感染症. 日本医学館, 1997.
8) 高橋公太:論座. 2021年2月23日
https://webronza.asahi.com/science/articles/2021022200005.html
9) Takahashi K:ABO-incompatible kidney transplantation. Elsevier, 2001.
10) 伊達洋圭:日医雑誌. 2022;151;1833-6.
11) 高橋公太:医事新報. 2022;5145:30-6.
https://www.jmedj.co.jp/journal/paper/detail.php?id=20734
12) 高橋公太:医事新報. 2021;5053:54.
https://www.jmedj.co.jp/journal/paper/detail.php?id=16586
13) 高橋公太:医事新報. 2021;5055:65.
https://www.jmedj.co.jp/journal/paper/detail.php?id=16633
14) 髙橋公太:医事新報. 2021;5077:29-37.
https://www.jmedj.co.jp/journal/paper/detail.php?id=17681
15) 高橋公太:医事新報. 2021;5092:27-33.
https://www.jmedj.co.jp/journal/paper/detail.php?id=18367
16) 北岡裕子:m3.com. 2020年12月14日
https://www.m3.com/clinical/open/news/853694
17) 細川芳文:都医雑誌. 2020;73:9-11.
18) To KK, et al:Lancet Infect Dis. 2020;20:565-74.
19) 高橋公太:医事新報. 2022;5133:35-8.
https://www.jmedj.co.jp/journal/paper/detail.php?id=19686
20) Recovery Collaborative Group:N Engl J Med. 2021;384:693-704.
21) 高橋公太:医事新報. 2022;5148:32-7.
https://www.jmedj.co.jp/journal/paper/detail.php?id=19688
22) 髙橋公太:腎と透析. 2021;90:289-301.
23) 高橋公太:臓器移植と感染─腎移植を中心に. 外科領域感染症. 酒井克治, 編. 医薬ジャーナル社, 1986, p249-73.
24) 高橋公太:腎移植患者と感染. 化学療法と腎臓. 上田泰, 他, 編. 東京医学社, 1992, p127-47.
25) 高橋公太, 他:移植. 1986;20(Suppl):490-500.
26) 高橋公太, 他:腎と透析. 1993;34:231-7.
27) 高橋公太:医事新報. 2021年7月21日. Web配信
https://www.jmedj.co.jp/journal/paper/detail.php?id=17678













































