お知らせ
(4)知っておきたい睡眠薬の知識[特集:眠れない患者に対応する]

ライフスタイル調整,睡眠薬への懸念の解消,適正服薬時刻の遵守が前提。
不眠のタイプと薬剤の薬理学的や薬物動態学的な作用特性を合わせる。

初期投与は非ベンゾジアゼピン系睡眠薬(非BZD)単剤から始め,その後用量調整が推奨される。
薬剤効果は不眠症状でなく,日中のQOL改善を目標とする。
減薬,休薬は計画的に行う。
リズム異常があれば,メラトニン受容体作動薬を考慮する。
『睡眠薬の適正な使用と休薬のための診療ガイドライン─出口を見据えた不眠医療マニュアル』1)を活用する。
1. ベンゾジアゼピン受容体作動薬(BZA)
1 開発の経緯
中枢神経ではγ─アミノ酸(γ─aminobutyric acid:GABA)が抑制性神経伝達物質として作用し,GABAa受容体に結合してCl−チャネルが開口する。その結果Cl−が細胞内に流入し,神経細胞膜に過分極が生じて興奮性の脱分極は低下し,神経興奮が抑制される。脳全体に存在する数百万のニューロンのうち約30〜40%がGABAに反応するため,GABAは脳に全般的な鎮静作用をもたらす。
20世紀初頭から使用されていたバルビツレート酸(barbiturate:BB)系睡眠薬は,GABAa受容体のBB結合部位に結合し,GABAを介さず直接Cl−チャネルを開口する作用があった。このため大脳皮質や脳幹網様体に作用し,耐性や依存性,大量服用時の呼吸抑制,激しい退薬症候などの欠点が問題となった。
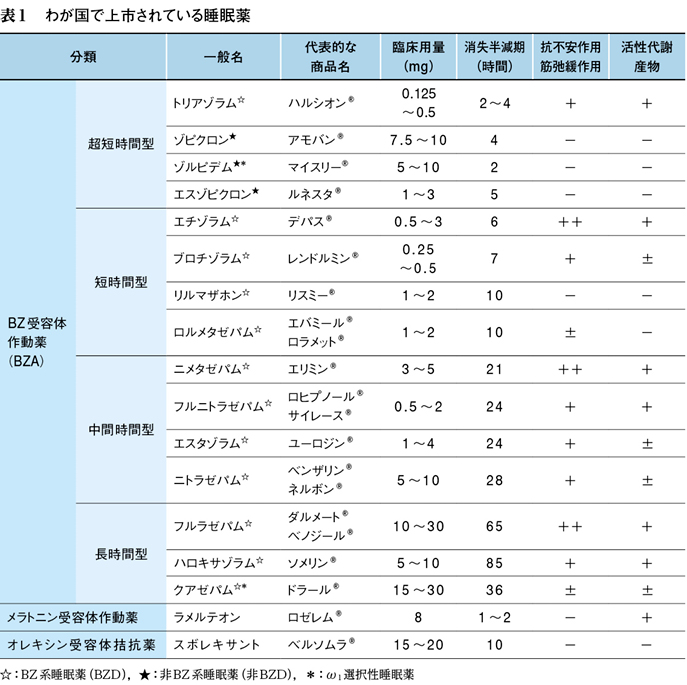
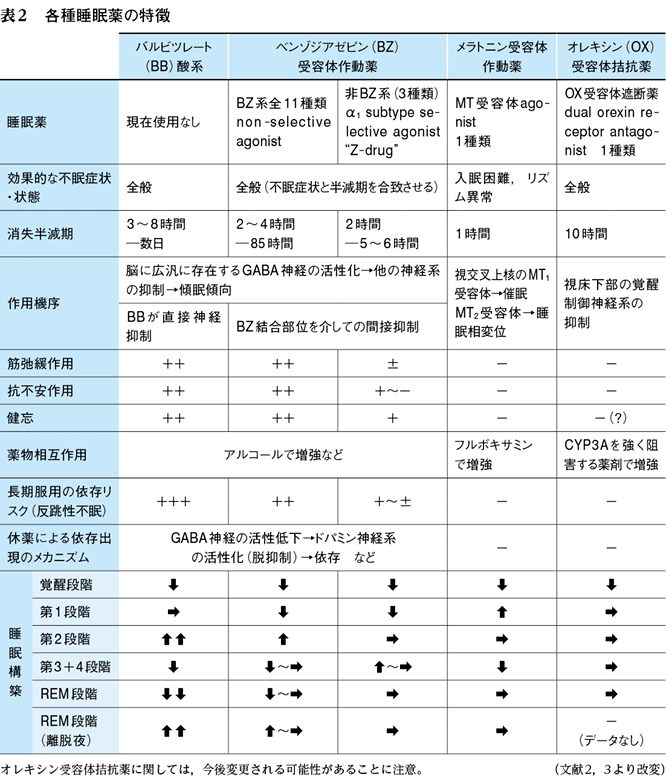
これを克服すべく,化学構造式にベンゾジアゼピン(benzodiazepine:BZ)骨格を持つBZ系睡眠薬(BZD)が登場し,不眠症の薬物療法の主流となった。1980年代には,睡眠薬としてさらに改良が行われ,BZ骨格でないものの,BZ受容体に作用する非BZ系睡眠薬(非BZD)が開発された。BZD,非BZDはともに,BZ受容体作動薬(benzodiazepine receptor agonist:BZA)として総称される(表1・22)3))。
2 薬理作用からみた臨床適応
BZAは,単独での結合ではGABAa受容体を活性化できず,その作用を示すには,視床下部と大脳辺縁系に集中するGABAa受容体のBZ結合部位に作用することが必要である。その結果,GABAa受容体のGABA結合能が亢進し,Cl−チャネルが開口して神経細胞の興奮抑制をもたらす。したがって,大量服用時にもBZ受容体が飽和されればそれ以上の神経抑制は起こらず,安全性が高い。これをアロステリック調節という。なお,GABAa受容体には,BZに結合部位だけでなく,アルコールの結合部位も存在する。
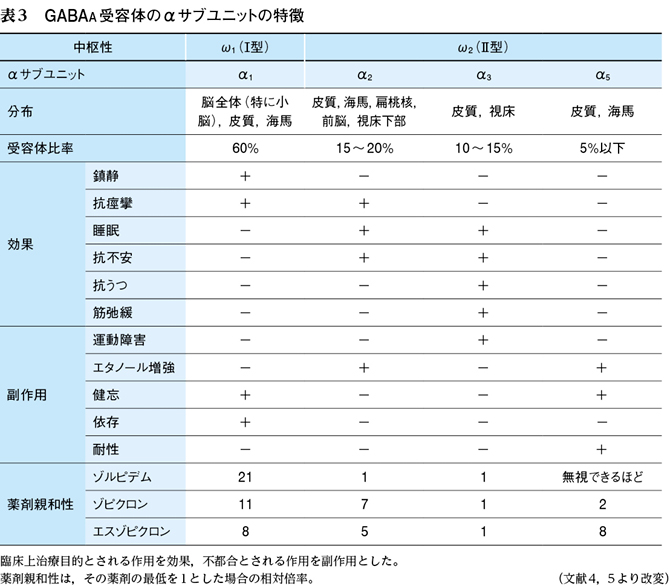
BZ結合部位は,2種の中枢型として大脳皮質や小脳,海馬に存在するω1(Ⅰ型)と線条体や脊髄に存在するω2(Ⅱ型)に分類される。またGABAa受容体は5個のサブユニットからなる五量体で,重要な役割を示すのがαサブユニットである。さらに,それはα1〜α6と分類され,α1は鎮静・催眠効果に関与し,α2は抗不安作用に関与,α2,α3は筋弛緩作用に関連する。そのほか,α3はドパミン神経系の機能調節,α5は記憶,学習に関与し,薬剤耐性にも関与する(表3)4)5)。ほとんどのBZDはα1,α2に非選択的に作用するため,筋弛緩作用による運動機能低下のほか耐性や中止後の反跳性不眠(52ページ参照)などの問題が残った。
近年,α1選択性の高い薬剤として,BZDのクアゼパム(ドラール®)やZ系睡眠薬(“Z-drug”:英語表記した場合に頭文字にZが多い非BZDの通称)と言われる非BZDのゾルピデム(マイスリー®),ゾピクロン(アモバン®),エスゾピクロン(ルネスタ®),ザレプロン(国内未承認薬)が開発されている4)。これらの薬剤は抗不安作用,筋弛緩作用が比較的弱く,高齢者の転倒や睡眠呼吸障害の対策上,利便性が高い。ただ,わが国の健康保険適用上,クアゼパムは睡眠時無呼吸症候群(SAS)には禁忌となっている。
プラセボを陵駕する効果(エフェクトサイズ,睡眠までの時間)を比較すると,主観的評価でBZD(−19.6分vs.−17分),客観的評価で非BZD(-10.0分vs.-12.8分)の効果が優勢だったが,いずれも有意差はなく,睡眠潜時に対する影響に大差はないと思われる6)。終夜睡眠ポリグラフ検査の検討では,BZDの多くは睡眠第2段階を増加させ,徐波睡眠には影響しないか減少させるのに対し,ゾルピデム(マイスリー®)はBZDに比べ徐波睡眠を有意に増加させる。加えて,BZDはREM睡眠を抑制するのに対して,ゾルピデム(マイスリー®)は抑制しない。反跳性不眠で悪夢を伴うのは,BZDのこのような作用特性に起因する。ただし,不眠症患者において,徐波睡眠の増加作用と臨床的効果の関係性は明確ではない。

残り7,537文字あります
会員登録頂くことで利用範囲が広がります。 » 会員登録する










































