お知らせ
新しい頭痛発症抑制薬「抗CGRPモノクローナル抗体」による片頭痛治療─フレマネズマブ発売後早期のリアルワールドデータ(3カ月投与も含めて)[学術論文]

2. フレマネズマブ
反復性片頭痛(episodic migraine:EM)患者875例を対象にした第3相臨床試験のHALO EM試験3)では,225mg 4週ごとの投与群(290例),675mg単回投与群(291例),プラセボ群(294名)にランダム化し,皮下注射(225mg 4週ごとの投与群では4週ごとに3回,675mg単回投与群では単回)を施行した(二重盲検期間:12週間)。主要評価項目は,初回投与開始後12週間の平均片頭痛日数のベースラインからの変化量とされ,225mg 4週ごとの投与群(-3.7日),675mg単回投与群(-3.4日),プラセボ群(-2.2日)であり,実薬群で有意な減少が認められた(P<0.001)。
慢性片頭痛(chronic migraine:CM)患者1130例を対象にしたHALO CM試験4)では,主要評価項目である初回投与開始後12週間の中等度以上の平均片頭痛日数のベースラインからの変化量は,675mg単回投与群(-4.3日),225mg 4週ごとの投与群(-4.6日),プラセボ群(-2.5日)であり,実薬群で有意な減少が認められた(P<0.001)。

これらの試験のpost hoc解析により,治療効果は投与後1週間の段階での発現が明らかにされている。さらに,CM患者への効果は,薬剤の使用過多による頭痛(medication overuse headache:MOH)の併存の有無に関係なく確認されている。
既存の2~4種の片頭痛予防薬が奏効しないEM/CM患者838例を対象にした第3b相臨床試験のFOCUS試験5)では,実薬群で有意な平均片頭痛日数の減少が認められている。日本人および韓国人のEM患者357例およびCM患者571例を対象に,HALO EM,HALO CMと同様の評価が行われ,いずれも実薬群の有効性が確認され,随伴症状に対しても実薬群での有効性がみられている6)7)。
フレマネズマブの臨床試験ではいずれも主な有害事象として注射部位反応がみられるが,重篤な有害事象の発現に関して群間差は認めておらず,日本人でも12カ月間のオープンラベル試験で長期安全性が確認されている8)。
3. ガイドライン
2021年8月に厚生労働省から「最適使用推進ガイドライン フレマネズマブ(遺伝子組換え)」9)が公表され,投与開始前3カ月以上において片頭痛日数が平均4日/月以上であり,既承認の発症抑制薬が,①効果不十分,②忍容性が低い,③禁忌や副作用から安全性への強い懸念がある,などの理由によって使用できない場合に使用が可能である。
日本頭痛学会においても「CGRP関連新規片頭痛治療薬ガイドライン(暫定版)」を公表し,4週間に1回投与の場合は投与開始後3カ月(3回投与後),12週間に1回投与の場合は投与開始後3カ月(1回投与後)または6カ月(2回投与後)を目安に治療上の有益性を評価し,症状改善が認められない場合には,投与中止を考慮することなどを推奨している10)。
片頭痛患者への実際の使用にあたっては,これらのガイドラインを遵守するように努める必要がある。また,無効例の存在や有害事象,薬価などについても丁寧に説明する必要がある。
4. 富永病院頭痛センターにおけるフレマネズマブの使用経験
富永病院頭痛センターでは,頭痛専門医は常勤7名,非常勤1名で急性頭痛から慢性頭痛まで幅広く頭痛性疾患を診療している。2010年の開設以来,年間1000例以上の頭痛患者を診療している。その約半数が片頭痛で,CM,MOHが多い。今回,2021年8月30日の発売から2022年3月末までの約7カ月間の成人の片頭痛患者で,フレマネズマブを使用した症例について後方視的に分析した。
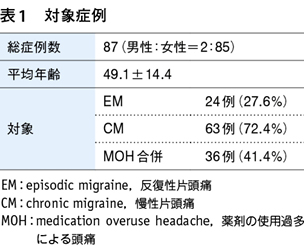
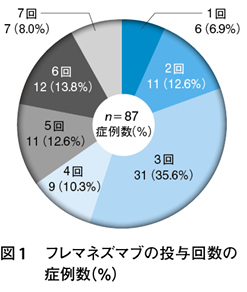
対象症例は計87例で,女性が85例(97.7%),CMが63例(72.4%)で,36例(41.4%)がMOHを合併していた(表1)。フレマネズマブは最大で7回まで投与されている(図1)。87例のうち,CGRP関連抗体薬として,最初にフレマネズマブが投与された症例が62例(71.3%),他薬剤からの切替例が25例(28.7%)であった(表2)。そのうち23例は前投与薬の無効~効果不十分が要因の変更であった。ほか1例はガルカネズマブの有効性はみられたが,注射部位反応のためにフレマネズマブに変更され,もう1例はエレヌマブで著明改善であったが,3カ月投与の希望があったため,フレマネズマブに変更された。

患者申告および医師判断による有効性は,「著明改善」が14例(16.5%),「有効」が33例(38.8%)であった。「やや有効」まで含めた有効例は68例(80.0%),初回例に限れば88.7%であった(表3)。直接の比較はできないが,「やや有効」以上の割合は当センターで報告した先行のガルカネズマブ(77.0%),エレヌマブ(73.7%)とほぼ同等である11)12)。 切替例でも56.5%において有効性が確認され,前投与薬が無効例~低反応例であっても一定の効果がみられており,ガルカネズマブ,フレマネズマブの同じ抗CGRP抗体薬間でのブランド変更も考慮可能であることが示唆された。