お知らせ
第2章|臓器の老化とフレイル・ロコモ 6 内分泌系の老化とフレイル・ロコモ 福岡秀規
- 登録日:
- 2024-08-01
- 最終更新日:
- 2024-08-01
![]()
●アンドロゲン,成長ホルモン(GH)は老化とともに分泌低下がプログラミングされたホルモンであり,フレイル・ロコモとの関連が示唆される。
●アンドロゲンの分泌低下症は筋量低下,歩行速度低下,骨密度低下,うつ症状などと関連し,その補充療法による改善が期待される。
●GHの分泌低下症ではメタボリックシンドローム,筋肉量減少,骨密度低下を呈し,その補充療法での改善が示されている。
●慢性的なグルココルチコイド過剰がフレイル・ロコモと関連することは明白であるが,老化による分泌量の変化は明らかでない。
フレイル・ロコモと関連する内分泌系
内分泌系の特徴のひとつとして,年齢とともに厳密にその分泌パターンがプログラミングされているホルモンが存在することが挙げられる。思春期にその分泌ピークを迎え,その後年齢とともに低下することがプログラミングされた代表的なホルモンとして,性腺ホルモン,成長ホルモン(growth hormone:GH)がある。これらの分泌制御は,主に視床下部が担っていると考えられている。この点から,老化に伴い抵抗力が弱まり体力が低下した状態であるフレイルと,老化による分泌低下が規定されているこれらのホルモンは,重要な関連性が示唆される。
内分泌系は,脳,免疫系,骨格筋,さらに心血管系,呼吸器系,腎,血液系への作用を介してフレイルと関連していると現在は考えられている1)。また,ホルモンの生理的な分泌低下だけではなく,病態としてのホルモン分泌不全症,ホルモン過剰症,ホルモン製剤の薬理量投与などがフレイル,ならびに運動器の機能が低下して移動が不自由となった状態であるロコモと関連することも特筆すべき点である。
本項ではその中でも,フレイル・ロコモとの関連が深いと考えられる内分泌系として,アンドロゲン,GHとその下流で蛋白合成を担うインスリン様成長因子Ⅰ(insulin-like growth factor-Ⅰ:IGF-Ⅰ),そしてグルココルチコイド(GC)について取り上げる。
アンドロゲンとフレイル・ロコモ
男性におけるアンドロゲンの主な由来は視床下部–下垂体系の刺激によって精巣から産生されるテストステロンである。視床下部でパルス状に分泌される黄体形成ホルモン放出ホルモン(luteinizig hormone-releasing hormone:LHRH)が下垂体門脈を介して下垂体前葉に到達し,黄体形成ホルモン(luteinizig hormone:LH)が分泌される。循環血液を介してLHが精巣に到達し,ライディッヒ細胞でテストステロンを合成分泌する。これが,男性における血中テストステロンの90%を占める。その他,副腎皮質からもデヒドロエピアンドロステロン(dehydroepiandrosterone:DHEA)およびアンドロステンジオンなどの副腎アンドロゲンが分泌される。これは,女性における主な血中アンドロゲンの由来である。副腎アンドロゲンも視床下部〔コルチコトロピン放出ホルモン(corticotropin-releasing factor:CRH)〕–下垂体〔副腎皮質刺激ホルモン(adrenocorticotropic hormone:ACTH)〕系により分泌調整がなされている。老化に伴うアンドロゲンの分泌低下はアンドロポーズとして知られ,血中の,特に遊離テストステロン濃度は思春期から経年的に低下することが知られている。
アンドロゲンは骨格筋におけるアンドロゲン受容体(androgen receptor:AR)を介して筋肉増強作用を呈するが,筋肉でのIGF-Ⅰ合成を介した作用も知られている。骨に対しては,むしろアロマターゼによって変換されたエストロゲンによる破骨細胞を介した作用がその主軸と考えられているが,骨芽細胞へのARを介した作用も知られている。また,アンドロゲンは脳にも作用しており,その低下は抑うつ,活力の低下と関連していることが報告されている。このことから,加齢とともに低下するテストステロン分泌がフレイルと関連していることが示唆されるが,これまでの知見では,主に男性性腺機能低下症による検討がなされている2,3)。男性性腺機能低下症の原因は多彩で,原発性(精巣障害)と続発性(視床下部/下垂体障害)があり,それぞれ先天性と後天性にさらに分けて示すことができる。その原因疾患として代表的なものを表1 2)に示す。
男性性腺機能低下症は,筋量低下,歩行速度低下,骨密度低下,うつ症状などと関連するという報告がある一方,血中テストステロン値との関連性については見解が一定していない2)。

男性性腺機能低下症におけるテストステロン補充療法(testosterone replacement therapy:TRT)について,わが国でランダム化比較試験(randomized controlled trial:RCT)「EARTH(effects of testosterone replacement therapy on metabolic syndrome among Japanese hypogonadal men)study」が行われ,下肢筋量の増加が示されている3)。しかし,TRTの筋力増強効果についてはいまだ結論に至っておらず,更なる検討が求められる。その他,うつ病に対する改善効果もRCTのシステマティックレビューとメタアナリシスにより性腺機能低下症患者に対しては認めることが示されている2)。
アンドロゲンがフレイル・ロコモと関連することを示唆する知見は,近年の前立腺癌に対する内分泌療法であるアンドロゲン除去療法(androgen deprivation therapy:ADT)の発展により,さらに明らかとなってきている。ADTは筋肉量減少,体脂肪増加と関連し,メタボリックシンドローム発症,骨密度低下とも関連する2)。以上のことから,アンドロゲンはフレイル・ロコモと関連するホルモンとしての認識が必要であり,特にその病的な分泌低下において注意が必要であると考える。
GH–IGF-I系とフレイル・ロコモ
GHは主に視床下部のGH放出ホルモン(GH-releasing hormone:GHRH)による刺激とソマトスタチンによる抑制により分泌が制御されている。さらに下垂体細胞に発現し,強力なGH分泌刺激作用を持つ成長ホルモン促進因子(GH secretagogue:GHS)受容体の内因性リガンドがグレリンであり,これは寒川,児島らによって胃から同定された。GHはSTAT5を介してアナボリックホルモンであるIGF-Ⅰを合成分泌し,これが主に肝臓から血中に分泌されるエンドクライン作用,ならびに各末梢組織でのオートクライン,パラクライン作用を介して骨の成長,骨密度維持,ならびに筋肉合成などを担っている。一方,脂肪では脂肪分解が起こるが,これは主にGHの作用と考えられる。また,GH–IGF-Ⅰ系の脳に対する直接作用も知られている(図1)。
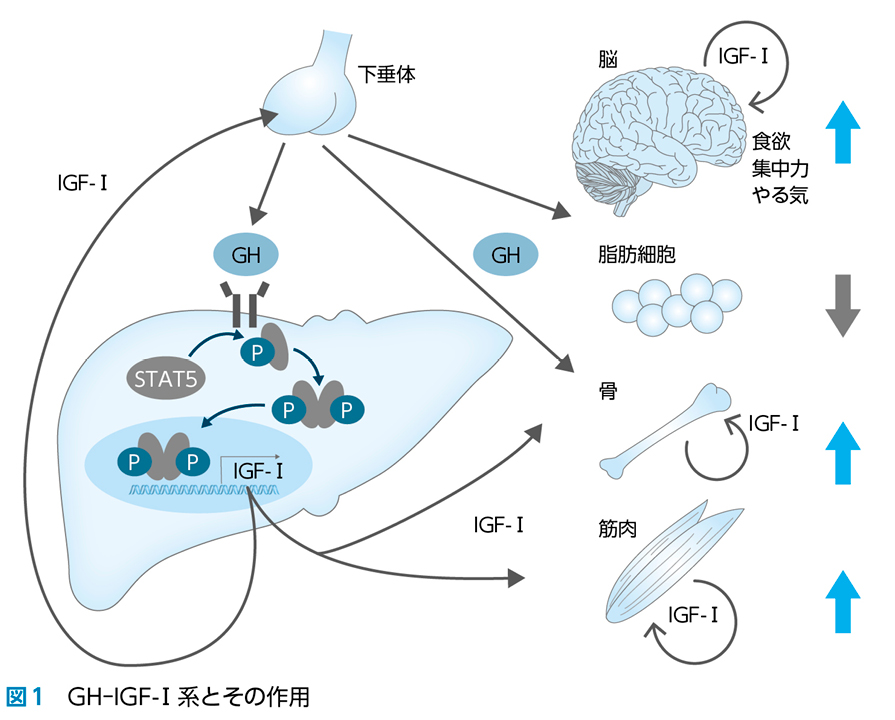
老化とともに,血中GH値,IGF-Ⅰ値は低下の一途をたどるが,これはソマトポーズと呼ばれ,主に視床下部のGHRHニューロンによって規定されている。GH分泌低下と平行して筋肉量の低下,内臓脂肪蓄積,骨密度低下が生じると考えられ,血中IGF-Ⅰ値の低下が高齢者における骨折リスクと関連していることが示されている4)。これは,骨密度低下だけではなく,筋肉量低下などによる転倒リスクも影響していることが考えられる。しかし,閉経後女性に対するGH治療のメタアナリスでは,骨密度上昇効果は明らかでないものの,骨折リスクの低減効果を認めることが示されている。しかし,健常高齢者に対するGH投与による筋肉量や骨密度の維持効果は現在証明されていない。
一方,鞍部腫瘤や放射線照射,頭部外傷などによりGH分泌不全症を呈した場合には,明らかに年齢に比して内臓脂肪が蓄積し,メタボリックシンドロームを呈すること,さらに筋肉量減少,骨密度低下を呈することが示されており,GH低下がこれらに寄与することは明白である。さらに,GH分泌不全症患者に対するGH補充療法は,内臓脂肪を減少し,筋肉量の増大,骨密度の上昇効果を呈することが示されている3~5)。このことから,経年的なGH低下はフレイル・ロコモと関連している可能性がある。
GCとフレイル・ロコモ
GCは視床下部–下垂体系によって制御され,副腎皮質から分泌されるステロイドホルモンであり,その分泌は日内変動パターンを呈する。慢性的なGC過剰を呈するクッシング症候群や薬理量のGC長期投与では,免疫能の低下,筋萎縮,骨密度低下とともに骨強度の著明な低下,うつ状態を中心とした様々な精神異常を呈することから,フレイル・ロコモとの関連が強く示唆される。また,近年ではGCの軽度自律性分泌を認めるサブクリニカルクッシング症候群においても,メタボリックシンドロームや骨密度低下,うつ指数の上昇を呈することが知られている。GCの老化による分泌量の変化は明らかでないが,日内変動の鈍化,コルチゾール分泌抑制の低下,ストレス反応からの回復遅延などが関連すると報告されており6),加齢との関連性については更なる検討が必要である。
文 献
1) Clegg A, et al:Lancet Diabetes Endocrinol. 2018;6(9):743-52.
2) 男性の性腺機能低下症ガイドライン作成委員会:日内分泌会誌. 2022;98(Supple):1-142.
3) 間脳下垂体機能障害と先天性腎性尿崩症および関連疾患の診療ガイドライン作成委員会:日内分泌会誌. 2023;99(Supple):1-171.
4) Mazziotti G, et al:Nat Rev Endocrinol. 2022;18(6):353-65.
5) Melmed S:N Engl J Med. 2019;380(26):2551-62.
6) Gaffey AE, et al:Neurosci Biobehav Rev. 2016;68:928-45.
































