お知らせ
学会レポート─2018年米国心臓病学会(ACC 2018)[J-CLEAR通信(92)]

2018年3月10日から3日間,米国オレンジカウンティ·コンベンションセンター(フロリダ)において,第67回米国心臓病学会(American College of Cardiology:ACC)が開催された。大規模試験の結果を中心に紹介したい。
1 CV高リスク痛風例へのフェブキソスタットによるCVイベント抑制はアロプリノールに非劣性も,CV死亡リスクは有意に増加:CARES試験
新しい尿酸低下薬であるフェブキソスタットは,古典的低下薬であるアロプリノールに比べ心血管系(CV)イベントの多い傾向が,第Ⅲ相試験で観察されていた。そのため米国FDAは,同薬のCV安全性を確認する大規模ランダム試験を要求した。それに応えて行われたのが,本学会で報告されたCARES試験である。フェブキソスタットによる脳心血管イベント抑制作用はアロプリノールに非劣性だが,CV死亡と総死亡のリスクは有意に増加していた。コネチカット大学のWilliam B. White氏が報告した1)。

(1)CKDステージ1~3で血管疾患合併の痛風例が対象
本試験の対象は,脳・心・脚の血管疾患,または糖尿病性血管症を合併する,痛風(米国リウマチ学会基準)患者6190例である。「クレアチニン・クリアランス<30mL/分」例は除外されている。平均年齢は約65歳で,尿酸平均値は8.7mg/dL,痛風罹患期間平均値は12年だった。腎機能に関しては,53%がステージ3の慢性腎臓病(CKD)だった。また62%が,試験前から尿酸低下薬を服用していた(うち91%はアロプリノール)。
これら6190例はフェブキソスタット群とアロプリノール群に無作為化され,二重盲検法で追跡された。フェブキソスタットは40mg/日,アロプリノールは腎機能に応じて200mg/日,あるいは300mg/日で開始し,試験開始2週間後に尿酸値が「6.0mg/dL未満」に達していなければ,両剤とも増量した。心血管系保護薬の服用率は,両群で同等だった。
(2)1次評価項目はアロプリノールに非劣性も,CV死亡リスク増加
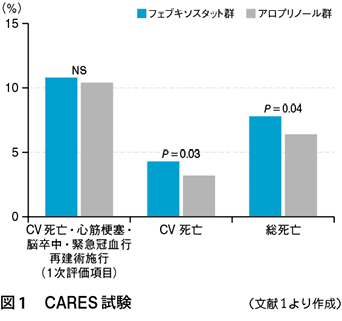
その結果,平均2.5年間以上の追跡期間中,1次評価項目である「CV死亡・心筋梗塞・脳卒中・緊急冠血行再建術施行」の発生率はフェブキソスタット群で10.8%となり(図1),アロプリノール群(10.4%)に非劣性であることが証明された。なお,尿酸値「<6mg/dL」「<5mg/dL」達成率はフェブキソスタット群のほうが高かった。
その一方,2次評価項目である「CV死亡」のリスクは,フェブキソスタット群で有意な増加が認められた(図1)〔ハザード比(HR):1.34,95%信頼区間(CI):1.03~1.73〕。両群のカプランマイヤー曲線は,試験開始30カ月後頃から乖離しはじめ,差は終了時まで広がり続けた。中でも心臓突然死の増加が目を引いた(2.7% vs. 1.8%)。しかし血中カリウムを含む電解質は,試験期間を通じ,両群間で有意差はなかったという。血圧や脂質代謝,腎機能も同様である。なお,冠動脈イベント(非致死性心筋梗塞・不安定狭心症による緊急血行再建)の発生率は,フェブキソスタット群5.2%,アロプリノール群5.6%だった。
(3)ITT解析だけでなくon-treatment解析でも同様の結果
ただしこれはintention-to-treat(ITT)解析の結果である。本試験は,脱落率が57%と高かった(群間に有意差なし)。そのため,試験薬を服薬中,ないし服薬中止後30日以内のCV死亡についても,比較が行われた(on-treatment解析)。しかし,やはりフェブキソスタット群において,リスクの有意増加が認められた(HR:1.49,95%CI:1.01~2.22)。CV死亡リスク増加の原因については,現在,解析中だという。
本試験は武田グローバル研究開発センター株式会社からの資金提供を受けた。
プレミアム会員向けコンテンツです(期間限定で無料会員も閲覧可)
→ログインした状態で続きを読む