お知らせ
FOCUS:C型肝炎克服時代の現状と残された課題


私が伝えたいこと
◉C型肝炎のウイルス検査の結果をまず確認する。
◉陽性の場合は,精査の上,直接作用型抗ウイルス薬(DAA)治療を行う。
◉ウイルス排除後も,病態に応じたフォローアップを行う。
目次
❶ C型肝炎治療の現況
C型肝炎ウイルス(HCV)は1989年に発見されたが,その後,きわめて早い時期(1992年)にインターフェロン治療が承認された。当初のインターフェロン治療は治療期間が24週に限定されており,治療効果にも限界があった。しかし,その後,治療期間の延長,リバビリンの併用,ペグ化製剤の開発などを経て,2000年代に入るとペグインターフェロン+リバビリン併用治療が標準治療として確立した。治療開始後のウイルス量の低下を指標にして投与期間を延長するという「レスポンスガイド」の概念も取り入れられ,6つある遺伝子型のうち遺伝子型1型で高ウイルス量の症例に対して約50%,その他の症例では約80%のウイルス排除率が達成されるようになった。
インターフェロンやリバビリンは,非特異的な抗ウイルス薬である。インターフェロンは1950年代に発見されたサイトカインのプロトタイプであり,様々な生物作用(抗ウイルス活性,抗腫瘍活性,免疫修飾作用)を有するが,もともと抗ウイルス活性を指標に発見された。リバビリンは,1970年代に合成された核酸型の抗ウイルス薬で,呼吸器感染症などの広い範囲のウイルスに対して抗ウイルス活性を有する薬剤である。
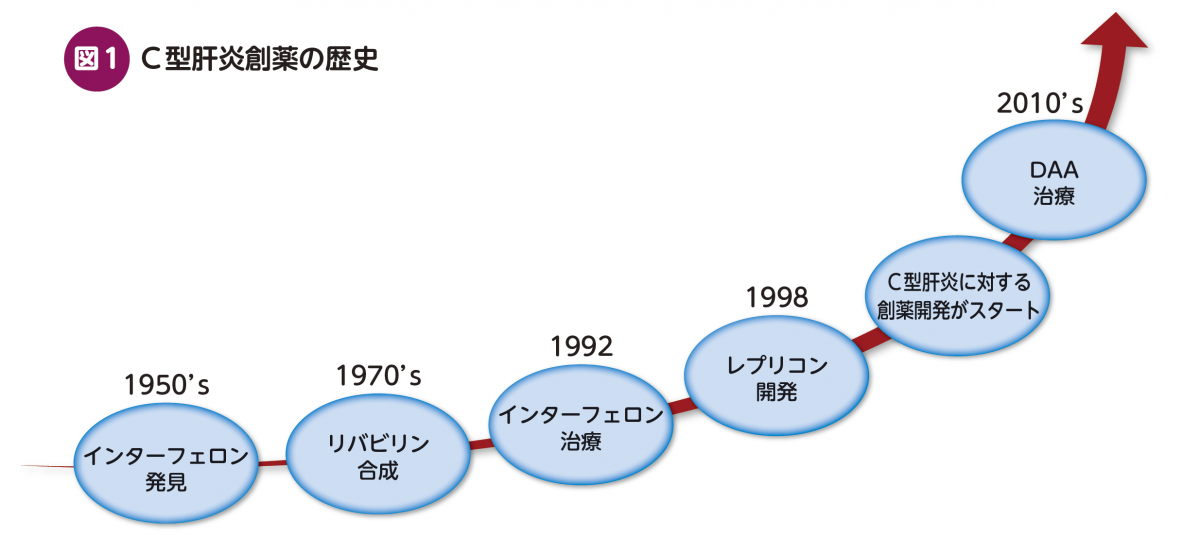
一方,HCVに対して特異的に作用する抗ウイルス薬の開発は,ウイルス発見にもかかわらず順調には進展しなかった。これはHCVの発見が遺伝子断片の発見であり,ウイルスそのものの分離・培養ではなかったためである。ウイルスの培養は困難をきわめたが,1998年にウイルスRNAの非構造領域を,インターフェロン応答の欠如した細胞にトランスフェクションすることにより,ウイルス増殖に必須な領域を細胞内で複製することが可能になった。これをレプリコンと呼んでおり,これを契機にC型肝炎に対する創薬開発が進展するようになった(図1)。
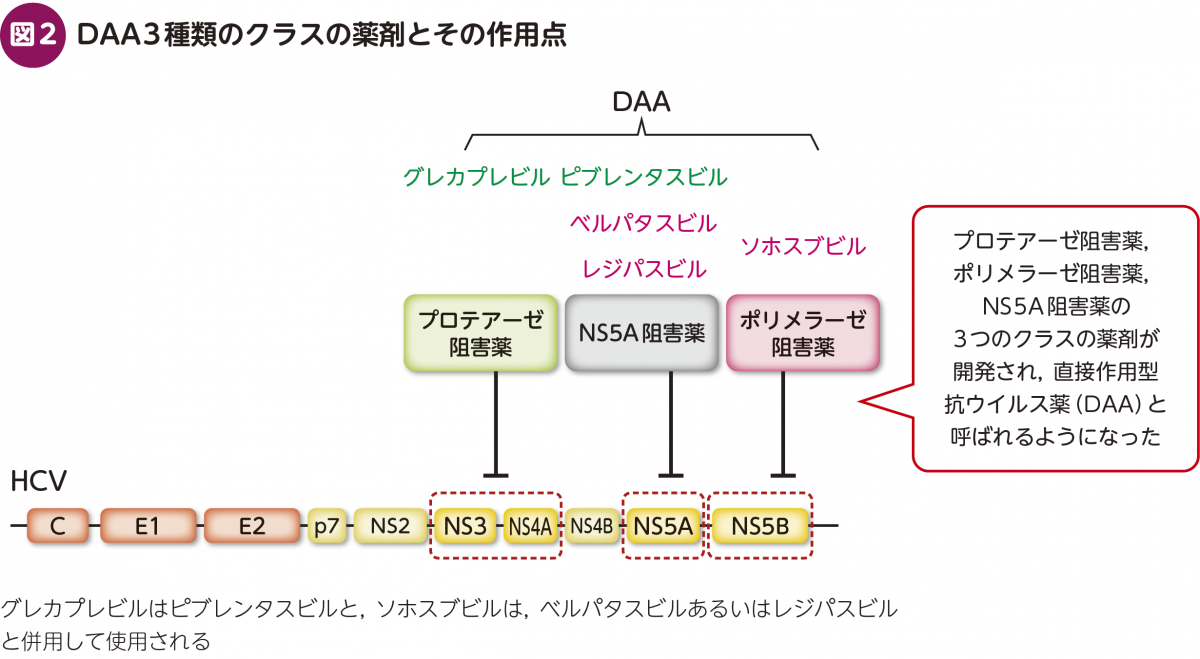
C型肝炎のウイルス増殖に必須な遺伝子は,非構造領域の中のプロテアーゼ,ポリメラーゼ,NS5A複製複合体である。最も早く開発されたのがプロテアーゼ阻害薬である。これはプロテアーゼの構造解析データからデザインされ,レプリコンを用いて改変された。ポリメラーゼ阻害薬は,核酸類似体の構造をもとに作製され,やはりレプリコンを用いて最適化された。NS5A複製複合体は,酵素活性を有さずその機能は当初不明であったが,レプリコンにおいて抗ウイルス活性を示す化合物を網羅的にスクリーニングする過程で,NS5A阻害薬は偶然発見された。NS5A複製複合体に変異が入ると活性が減弱することから,NS5A阻害薬であることが明らかになった。これらの3つのクラスの薬剤は,後に直接作用型抗ウイルス薬(direct acting antivirals:DAA)と呼称されるようになった(図2)。
最初に臨床に登場したのは,プロテアーゼ阻害薬である。2011年にペグインターフェロンやリバビリンと併用する3剤治療として用いられ,1型高ウイルス量症例に対するインターフェロン投与期間を短縮し,さらにそのウイルス排除率を80%に向上させる薬剤として画期的なものであった。プロテアーゼ阻害薬をインターフェロンやリバビリンと併用する理由は,単独で投与すると,高率にプロテアーゼ領域に変異を持ったウイルスが出現し,治療効果が得られなくなるためである。しかし,3剤治療をしても20%の症例で治療効果が得られず,このような症例には耐性ウイルスが出現し,その対策が問題となった。
プロテアーゼ阻害薬に続いて,NS5A阻害薬やポリメラーゼ阻害薬が臨床に登場し,複数のクラスの阻害薬を併用することにより,インターフェロンを用いなくても,薬剤耐性の出現を抑制し治療効果を高めることが可能になった。2014年に初めてのインターフェロンフリー治療として,プロテアーゼ阻害薬とNS5A阻害薬の併用治療が承認され,翌2015年にはポリメラーゼ阻害薬とNS5A阻害薬の併用治療が承認された。これにより,C型肝炎の治療はインターフェロン治療から真の意味でのDAA治療に置き換わることになった。その後,各クラスの薬剤がさらに改良されることにより,現在では12週の治療期間で95%以上の症例でウイルス排除が可能となった。
この10年間で10種類近くの新しい治療レジメンが承認されたが,その多くは古い世代の薬剤として既に臨床から退いている。現在使用可能な薬剤は,プロテアーゼ阻害薬とNS5A阻害薬の組み合わせであるグレカプレビル/ピブレンタスビル(マヴィレット®),ポリメラーゼ阻害薬とNS5A阻害薬の組み合わせであるソホスブビル/レジパスビル(ハーボニー®),ソホスブビル/ベルパタスビル(エプクルーサ®)である。ソホスブビル/レジパスビルは,2015年に登場した薬剤耐性バリアの高い画期的な薬剤であるが,ソホスブビル/ベルパタスビルがすべての病型のC型肝炎の治療に適応拡大された2022年以降,それに置き換えられ使用機会は減っている1)。
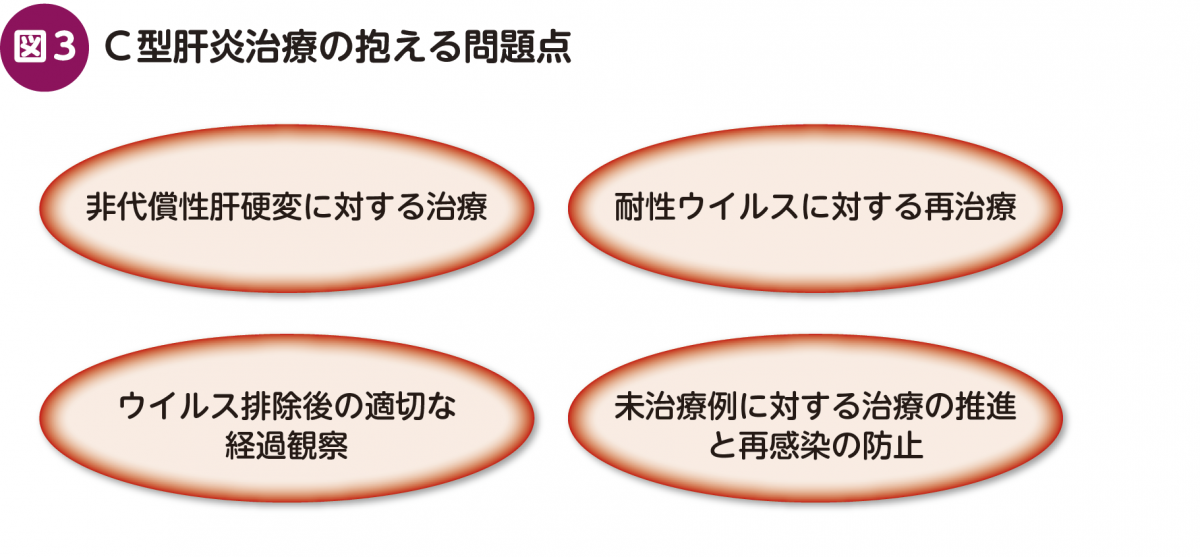
このような中で,現在問題になっているのは,①非代償性肝硬変に対する治療,②耐性ウイルスに対する再治療,③ウイルス排除後の適切な経過観察,④未治療例に対する治療の推進と再感染の防止である(図3)。
❷ 非代償性肝硬変に対する治療
(1) DAA治療の結果と予後
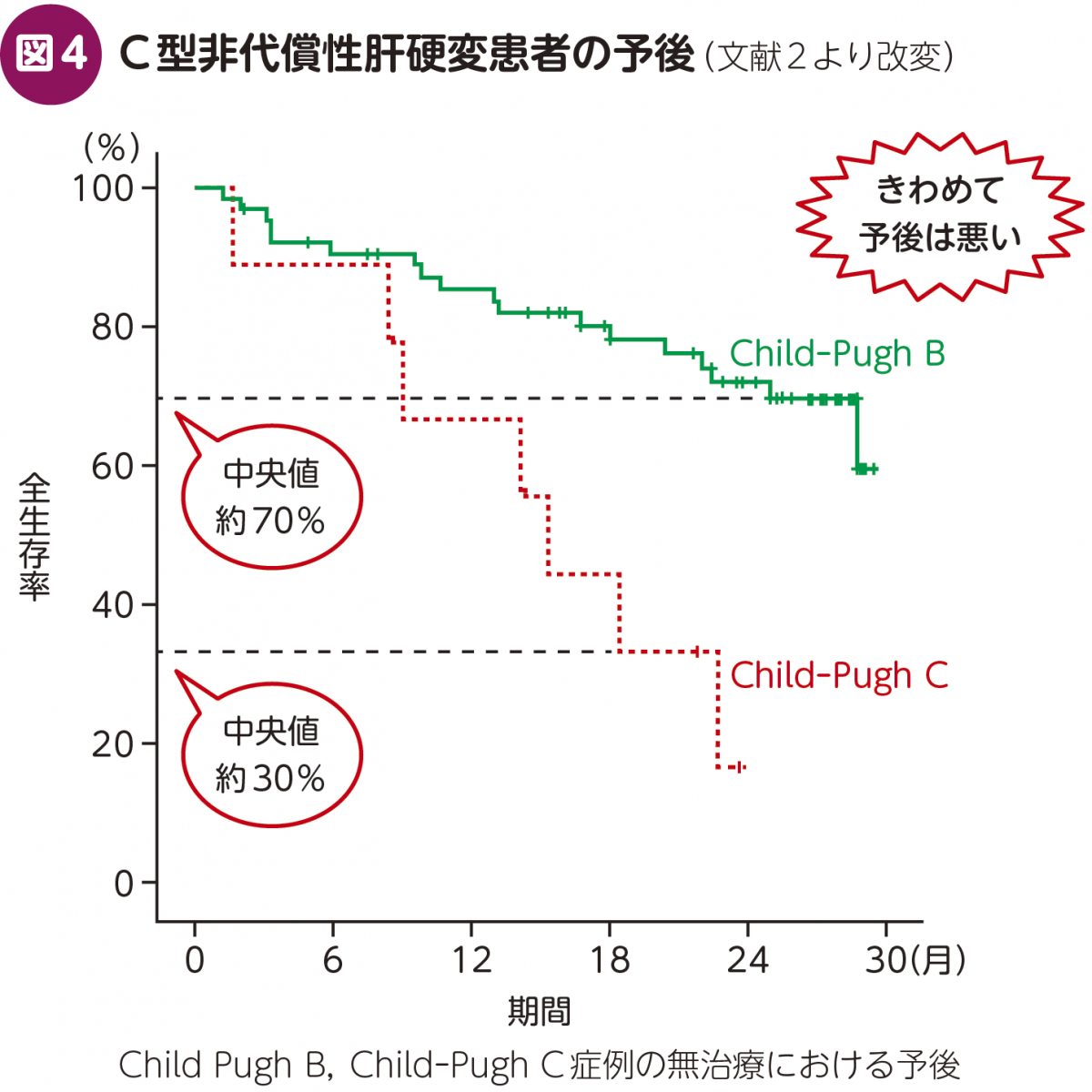
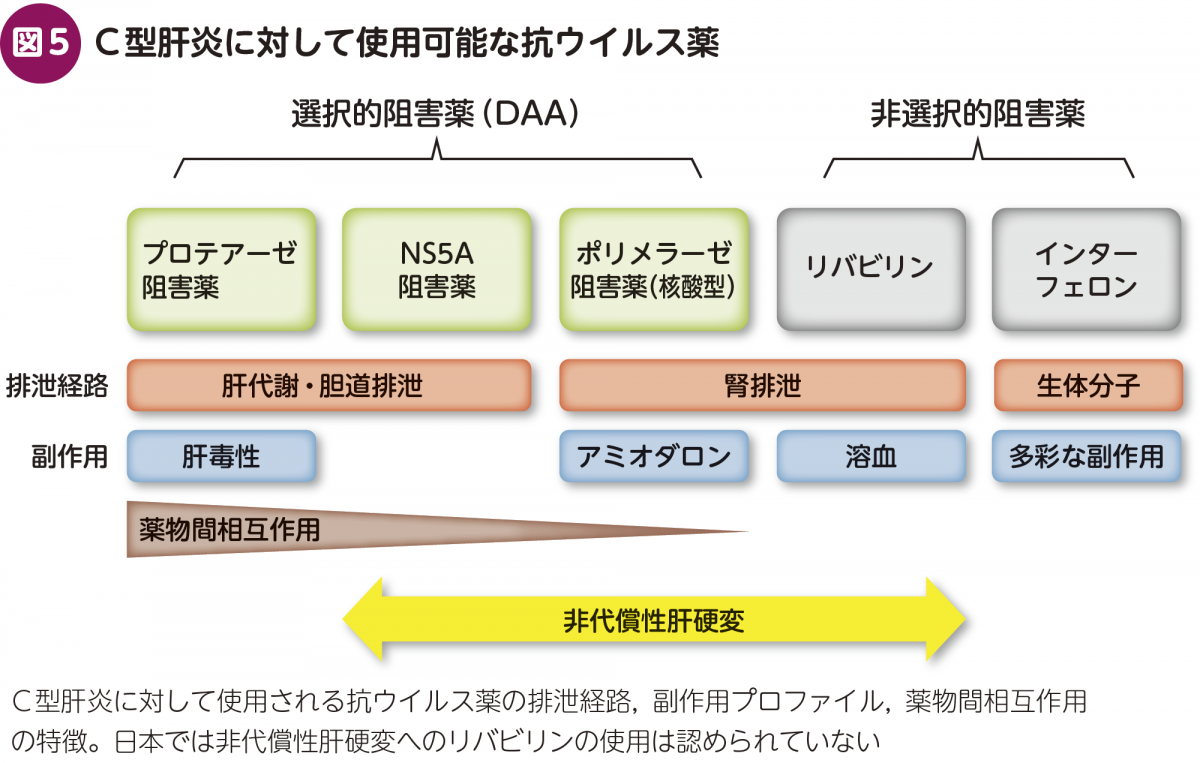
非代償性肝硬変は生存率の中央値が,Child-Pugh B症例で約70%,Child-Pugh C症例では約30%と,きわめて予後の悪い疾患である(図4)2)。インターフェロン治療の時代には,治療期間も長く,様々な副作用を有する抗ウイルス治療を,このような患者に適応することは想定もできなかった。DAA治療の時代になると,肝障害性の低いクラスのDAAを組み合わせることにより(図5),このような患者群に対しても抗ウイルス治療を行うことが可能となった。
日本ではC型非代償性肝硬変に対して,ソホスブビル(ポリメラーゼ阻害薬)とベルパタスビル(NS5A阻害薬)の12週投与がリバビリン併用群と非併用群の2群比較試験として実施され,ウイルス排除効果は両群間に差がないことが示された。この第3相臨床試験の結果を受けて,2019年に非代償性肝硬変に対するソホスブビル/ベルパタスビル12週投与が承認された。市販後の全国多施設研究の結果によると,ウイルス排除率はChild-Pugh B症例で93%,Child-Pugh C症例で83%であり,実臨床においても臨床試験とほぼ同等の治療効果が得られている。
治療終了時に,約3分の1の症例が,Child-Pugh Aに移行するが,その後の肝予備能の改善は少なくChild-Pugh Aに達するのは約半数にとどまる。一方,ウイルス排除後の肝癌については,初発例に限っても1年で7.1%,3年で17.5%の発がん率であり,きわめて高率である。また,入院を要する非代償性イベントの発生は1年で13.4%,3年で21.8%にみられている。
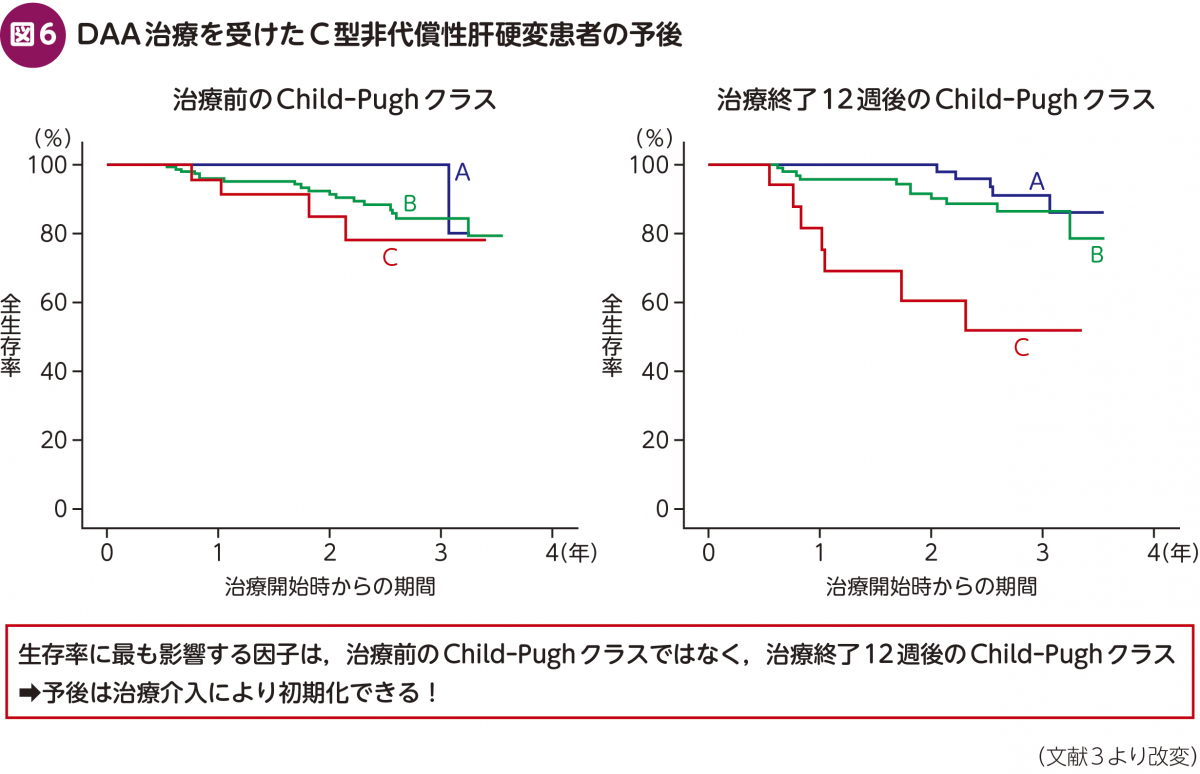
このようなデータは,非代償性肝硬変の予後が引き続き厳しいものであることを示しているが,未治療例やウイルス非排除例に比べると格段に予後は改善されており,治療開始時Child-Pugh B症例の2年生存率は91.2%,Child-Pugh C症例のそれは78.7%になっている。興味深いのは,生存率に最も影響する因子は,治療前のChild-Pughクラスではなく,治療終了時のそれであるということである(図6)3)。このことは非代償性肝硬変患者の予後が,治療介入により初期化できることを意味している。
(2) 門脈圧亢進症との関連
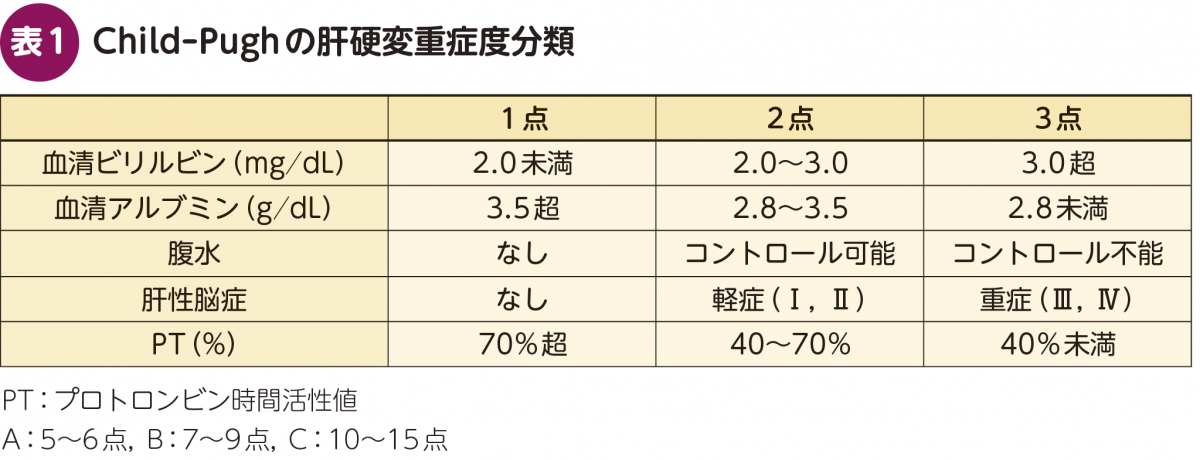
DAA治療を行っても予後の改善が得られにくい背景に何があるかは,十分には理解されていない。1つの可能性は門脈圧亢進症との関連である。Child-Pughクラスはもともと静脈瘤のリスクを評価するために開発された指標であり,門脈圧亢進症と一定の相関がある。しかし,同じChild-Pughクラスであっても,門脈大循環シャントの程度は様々である。
DAA治療を行うとアルブミン合成を中心とした肝機能は改善するが,いったん形成された門脈大循環シャントの可塑性は低いと考えられる。したがって,既にシャントを有する症例では,ウイルスが排除されても循環動態が改善されずむしろ徐々に悪化し,肝機能が低下していく可能性がある。C型肝炎のポイント・オブ・ノーリターンを明らかにすることは,その対策に直結する。今後さらなる検討が必要である。