お知らせ
(1)革新的治療と腫瘍マーカー[特集:腫瘍マーカーの実力]

腫瘍マーカーは,その時代時代の観察手段の開発とともに見出されてきた
がん診療の進歩は日進月歩であり,腫瘍マーカーに期待される役割も大きく変化してきた

従来,行われてきたがんの補助診断や,モニタリングのみならず,微小残存病変の検出,コンパニオン診断などの役割も,腫瘍マーカーにあると言える
多様ながんのマーカーを的確にとらえ最適な治療を提供する個別化医療がさらに進むと思われる
1. 腫瘍マーカーの現況
腫瘍マーカー(tumor marker)の定義は「がん細胞がつくる物質,または体内にがんがあることに反応して非がん細胞がつくる物質で,それらを組織,体液,排泄物などで検出することが,がんの存在,種類,進行の程度を知る上で目印となるもの」である1)。腫瘍マーカーはその時代時代の観察手段の開発とともに見出され,さらに,がん治療の進歩に合わせて期待される役割も年々変化してきている。
古くは,免疫電気泳動法により検出されるM蛋白やBence-Jones蛋白,その後,免疫化学的分析法により検出される胎児性蛋白などの腫瘍抗原,モノクローナル抗体により検出される糖鎖抗原や自己抗体が腫瘍マーカーとして普及し,がんの補助診断や,がん患者ならびにがん発生高リスク患者の経過観察に利用されてきた。近年は,ヒトゲノムやプロテオーム解析が進展するに伴い,疾病に関わる生体内分子の特定解析が進み,悪性腫瘍の増殖等に関連する標的分子が特定されつつあり,がん遺伝子やがん抑制遺伝子,ならびにその産物も腫瘍マーカーとして見出され,普及するに至った。
一方,近年,悪性腫瘍の増殖等に関連する生体内分子が特定されつつあり,それらを標的とした分子標的治療の開発が活発に進められ,腫瘍マーカーに期待される役割も年々変化してきている。新規治療薬が次々と登場し,従来の治療にない深い奏効も期待できる中,いかに残存病変を検出しうる分子腫瘍マーカーを開発できるかが肝要となっている。さらに,個別化医療という考えががん治療の主流となり,特定の医薬品の有効性や安全性をいっそう高めるためにあらかじめ検査するコンパニオン診断も,腫瘍マーカーの役割の一部となってきている。
本稿では,近年ますます加速するがん治療の変貌に合わせて,最近注目されている革新的治療薬と腫瘍マーカーとの関係を臨床に即して述べる。
2. がん分子標的治療と微小残存病変の評価
新しい治療法の開発により達成される深い奏効を的確に評価し,効果判定,治療方針の選択,予後予測に役立てる取り組みが進んでいる。遺伝子発現解析法による微小残存病変の評価が他がんに先んじて可能となり,効果判定と予後予測に必須となった疾患として,慢性骨髄性白血病(chronic myeloid leukemia:CML)を例示する。
CMLは,造血幹細胞レベルの細胞に染色体転座t(9;22)により形成されるBCR-ABL融合遺伝子が産生する恒常的活性化チロシンキナーゼにより,造血幹細胞に過剰な増殖がもたらされ発症する。従来の化学療法では急性転化期への進行によりほぼ全例が死亡し,同種造血幹細胞移植のみで治癒しうる疾患であったが,第一世代BCR-ABL融合遺伝子チロシンキナーゼ阻害薬(tyrosine kinase inhibitor:TKI)イマチニブの登場以降,わが国での承認が5剤そろい,長期の疾患コントロールと生存が可能となった2)。
図1に示すように,BCR-ABL融合遺伝子は腫瘍細胞と1:1で対応するため,BCR-ABL mRNAとABL mRNAを定量リアルタイムPCR(polymerase chain reaction)法で解析し,その比を国際標準値に変換することで微小残存病変を含む腫瘍量を推定でき,治療効果のモニタリングが可能となる。残存CML細胞数が108以下に相当する国際標準値に達すると分子遺伝学的大奏効と定義され,効果判定基準にも組み込まれており,その達成,維持により病期進行を確実に回避でき,予後を劇的に改善できる3)。さらに,残存CML細胞数が106~107以下に達すると分子遺伝学的完全奏効とされる。従来,TKIを中止すると完全寛解の維持は困難とされていたが,Stop Imatinib(STIM)試験では,イマチニブ投与により分子遺伝学的完全奏効を2年間保った症例の41%において,イマチニブの服用中止後1年間,分子遺伝学的完全奏効を維持できることが報告され4),現在は各国各施設においてさらなる検証が進められている。
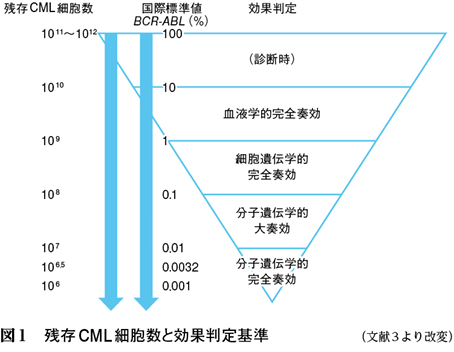
このように,CMLにおいては分子標的治療薬の奏効を評価するBCR-ABL mRNA定量解析により,効果判定,治療方針の選択,予後予測が可能となり,治癒の可能性を期待できるまでになっている。

残り3,621文字あります
会員登録頂くことで利用範囲が広がります。 » 会員登録する